הקשר הגנטי לניוון מקולרי גילי
בשנים האחרונות מתפרסמים מחקרים שמזהים השפעות של גנים על התפתחות והתקדמות של ניוון מקולרי גילי. לאור הממצאים, מומלץ לקרוביהם הביולוגים של חולים להקפיד על בדיקות עיניים אחת לשנה מגיל 50 לאיתור המחלה בשלבים מוקדמים

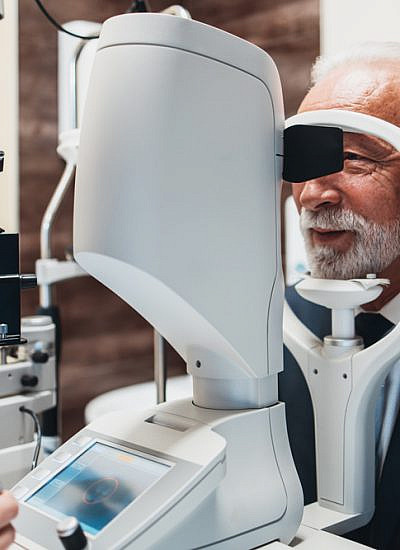
ניוון מקולרי גילי (נמ"ג) היא מחלת עיניים כרונית מתקדמת של מבוגרים מגיל 50 ומעלה, אשר נגרמת על רקע פגיעה ב'מקולה' – האזור מרכז הרשתית שאחראי על חדות הראייה והראייה לפרטים. המחלה מלווה בפגיעה מתקדמת בחדות הראייה, והיא מהווה כיום את הסיבה המרכזית לעיוורון בעולם המערבי וכן בישראל.
מחקרים מזהים בניוון מקולרי גילי מחלה רב גורמית, שמתפתחת כתוצאה משילוב בין נטייה גנטית, גורמים סביבתיים ותהליכי הזדקנות ביולוגיים. מחקר שפורסם ביוני 2025 בכתב העת Lancet Global Health מעריך כי מספר המתמודדים עם ניוון מקולרי, אשר מצוי במגמת עלייה ולפי הערכות עמד על 8.06 מיליון איש נכון לשנת 2021 – צפוי להמשיך ולהאמיר עד ל-21.34 מיליון מתושבי העולם בשנת 2050. העלייה בתחלואה מיוחסת בעיקר להזדקנות האוכלוסייה ולהיקפים נרחבים של עישון סיגריות, שהוכח כיום כגורם הסביבתי הניתן למניעה הראשון במעלה למחלה.
למרות שגיל מבוגר הוא גורם הסיכון המשמעותי ביותר לניוון מקולרי גילי, לגנטיקה ככל הנראה תרומה מכרעת לתחלואה, ונכון לתחילת שנת 2026 זיהו מדענים מעל ל-50 שינויים גנטיים (וריאנטים) שמגדילים את הסיכון להתפתחות של ניוון מקולרי.
ידיעה על קרובי משפחה ביולוגים שפיתחו ניוון מקולרי כבר אמורה להתריע היום בדבר הצורך לבצע בדיקות עיניים קבועות אחת לשנה כדי לאתר את מחלת העיניים בשלבים מוקדמים ולהתאים טיפולים שביכולתם לעכב את התקדמות המחלה ואת הידרדרות הראייה ועיוורון. במקביל נחקרים טיפולים מתקדמים לעיכוב המחלה המבוססים על שינויים גנטיים ספציפיים שנקשרו אליה.
הכתבה להלן מתייחסת להיבטים הקשורים בגנטיקה וניוון מקולרי גילי:
הקשר הגנטי-משפחתי לניוון מקולרי
לפי הערכות, ל-20% עד 30% מהאנשים עם ניוון מקולרי גילי יש קרובי משפחה שמתמודדים או התמודדו עם המחלה – מה שמצביע על השפעה גנטית חזקה בבסיס המחלה. לפי מחקרים, תורשה גנטית מסבירה כ-50% מהשונות בתחלואה בניוון מקולרי.
מחקר תאומים שבוצע בארה"ב ופורסם עוד ביולי 1994 בכתב העת JAMA Ophthalmology, הציג ראיות לכך שחרף השפעות סביבתיות שונות על התפתחות ניוון מקולרי גילי – הרי שניכרת גם השפעה גנטית על התפתחות המחלה אשר עשויה לעבור בתורשה בין הדורות.
חוקרים אמריקאים מאוניברסיטת מהרווארד פרסמו בנובמבר 2023 בכתב העת American Journal of Ophthalmology כי נוכחות של ניוון מקולרי גילי מעלה את הסיכון להתפתחות והתקדמות של המחלה ב-21% בהינתן קרוב משפחה אחד לחולה וב-55% בהינתן שני קרובי משפחה חולים או יותר.
שינויים גנטיים ספציפיים
לצד מחקרי משפחות, עד כה זוהו במחקרים מעל ל-50 שינויים גנטיים (וריאנטים) ספציפיים שנקשרו לעלייה בסיכון של ניוון מקולרי גילי ב-34 מיקומים שונים על הגנום, שחלקם עשויים לעבור בתורשה גנטית וחלקם עשויים להתפתח לפתע בדור מסוים ('דה נובו'). חלק מהגנים שנמצאו קשורים לניוון מקולרי גילי מקודדים לחלבונים שאחראים בין השאר על מטבוליזם של שומנים בדם, ייצור חלבון הקולגן, תיקון DNA, היקשרות חלבונים והפקת אותות תאיים. חשוב להבהיר כי איתור וריאנט שנקשר לסיכון מוגבר לניוון מקולרי גילי אינו מעיד בהכרח שהמחלה תפרוץ אצל המטופל, אלא רק כי הוא נמצא בסיכון גבוה יותר להתפתחותה.
במחקרים שעסקו בנושא בולטים שני סוגי שינויים ספציפיים, אשר נקשרו לסיכון גבוה בעשרות מונים הן להתפתחות של ניוון מקולרי והן להתקדמות המחלה לשלבים חמורים יותר:
(1) שינויים בקבוצת הגנים של מערכת המשלים הממוקמים על כרומוזום 1
המסלול בו נמצאו שינויים גנטיים רבים ביותר הוא מערכת המשלים (Complement System) – מערכת חלבונים בדם המהווים חלק ממערכת החיסון.
גנים אלה מהווים חלק חיוני ממערכת החיסון, ומגנים מפני פתוגנים פולשים, אך בווריאנטים מסוימים עלולים גם לפעול בטעות נגד תאים בריאים ובהם תאי הרשתית. חלק מהחוקרים סבורים שתהליכי דלקת ומנגנונים חיסוניים הם חלק מהגורמים להתפתחות ניוון מקולרי גילי, כאשר הקשר בין וריאנטים בגנים של מערכת המשלים לבין המחלה תומך בתיאוריה זו.
מבין קבוצת גנים זו, הגן CFH נחקר ביותר, כאשר נוכחותו של וריאנט ספציפי המסומן באותיות rs1061170 נקשרה באופן משמעותי למחלה. מחקר מהולנד אף מצא שמדובר בווריאנט שכיח למדי, אשר לפי הדיווח ביולי 2006 בכתב העת JAMA זוהה בקרב מעל לשליש (36.2%) מהנכללים במדגם של מבוגרים בגיל 55 ומעלה תושבי העיר רוטרדם. לפי מטה אנליזה שפורסמה באוגוסט 2006 בכתב העת Human Molecular Genetics, כשגן CFH הוא הטרוזיגוט – כלומר שיש לו אלל אחד תקין ואלל אחד וריאנטי – הסיכון לניוון מקולרי גילי גדל עד פי 2.5, וכשהגן הוא הומוזיגוט וריאנטי – כלומר ששני האללים שלו מכילים וריאנטים – הסיכון למחלת העיניים גדל עד פי 6 בהשוואה לאוכלוסייה הכללית. מחקר מפולין שפורסם במאי 2022 בכתב העת Medicina אף מצא כי נוכחות הווריאנט שכיחה יותר אצל מטופלים עם ניוון מקולרי רטוב שלא מגיבים באופן מיטבי לטיפולים בהזרקות תוך עיניות.
(2)הגן ARMS2 שכונה בעבר גם HTRA1, המצוי על כרומוזום 10
אף שקיים קשר חזק בין הגן לבין הסיכון להתפתחות ניוון מקולרי גילי, תפקידו המדויק בסיכון זה עדיין אינו ידוע לאשורו. מוטציות בגן ARMS2 שנקשרות לניוון מקולרי גילי שכיחות אף הן באוכלוסייה. נתונים ממחקר של קונצסרציום העיניים האירופי, שפורסמו ביולי 2022 בכתב העת Ophthalmology, זיהו את המוטציה השכיחה בקרב כשני שליש (65%) מהמאובחנים בשלבים מתקדמים של ניוון מקולרי גילי, וזו הייתה מלווה בסיכון גבוה פי 12.2 לאבחון בשלב המתקדם של מחלת העיניים ולסיכון גבוה פי 8.6 לסיבוך מסיכון אטרופיה גאוגרפית של ניוון מקולרי יבש.
וריאנטים נוספים
לצד השינויים בשני הגנים CHF ו-ARMS2, מחקרים בתחום רומזים כי שינויים בגנים נוספים שנקשרו למחלות עיניים שונות – עשויים אף הם להשתתף בתהליך ההתפתחות וההתקדמות של ניוון מקולרי גילי, למשל שינויים בגן RDS שנקשר בהתפתחות המחלה 'רטיניטיס פיגמנטוזה' (מחלת עיניים ניוונית שעוברת בתורשה ועלולה להוביל לעיוורון); ובגנים TIMP3 ו-EFEMP1 הקשורים במחלות שמשפיעות על לקויות ראייה הדומות לביטוי של ניוון מקולרי גילי.
מעבר לאלה, בספרות הרפואית מתועדים גם שינויים גנטיים נדירים המגדילים את הסיכון לניוון מקולרי גילי. חוקרים מהולנד וגרמניה תארו במארס 2016 בכתב העת JAMA Ophthalmology סיכון גבוה למחלה אצל מי שזוהו עם מוטציות נדירות בגנים שאחראים לפעילות מערכת המשלים, לרבות הגן CFH שתואר קודם וגנים נוספים (למשל CFI, C9 ו-C3).
לצד השינויים הגנטיים שנקשרים לניוון מקולרי גילי, מחקרים בשנים האחרונות מנסים להתחקות אחר וריאנטים גנטיים בעלי השפעה מגֵנה מפני ניוון מקולרי גילי שמפחיתים את הסיכון למחלה. כפי הידוע כיום, וריאנטים אלו כוללים שינויים בגנים מסוימים אחרים שמשתתפים בתפקוד מערכת המשלים ובגנים הקשורים בתפקוד המערכת החיסונית, וכן בגנים המשפיעים על חילוף שומנים בגוף.
בדיקות סקר לאבחון אנשים בסיכון
ההשלכות של זיהוי שינויים שמעלים את הסיכון לניוון מקולרי גילי באוכלוסייה הכללית עדיין שנויות במחלוקת, ונכון לתחילת שנת 2026, ארגונים מקצועיים מובילים כמו האקדמיה האמריקאית לרפואת עיניים (AAO) אינם ממליצים על ביצוע בדיקות גנטיות באוכלוסייה לאיתור מוטציות שמגדילות את הסיכון למחלה, בעיקר משום שגם אם בדיקה גנטית מראה כי קיימים וריאנטים גנטיים ספציפיים – אין כיום טיפול גני הזמין למניעה או לטיפול במחלה.
בדיקות גנטיות למוטציות הקשורות לניוון מקולרי עשויות להפוך לשימושיות בעתיד, עם פיתוח טיפולים חדשים המבוססים על גנוטיפים אישיים הקשורים למחלת הרשתית.

בדיקות גנטיות למאובחנים
בעידן הרפואה המותאמת אישית – יש רופאים שממליצים כבר היום לבצע בדיקות גנטיות למאובחנים עם ניוון מקולרי גילי כדי לנסות ולאתר שינויים גנטיים שעשויים להעלות את הסיכון להתקדמות מהירה של המחלה, לזהות חולים שמועדים יותר לעיוורון ולשים אצלם דגש יתר על היענות לטיפול התרופתי. עם זאת, רוב הארגונים בעולם בתחום רפואת העין אינם ממליצים כיום על ביצוע נרחב של בדיקות גנטיות לניוון מקולרי גילי גם לחולים – בעיקר על רקע המורכבות בתפקיד הגנטיקה בהתפתחות המחלה והתקדמותה.
יש לציין כי מתן אינדיקציה על סיכון גבוה להתקדמות המחלה הוא חשוב נוכח החשש מהיענות חלקית הזרקות התוך עיניות, כאשר מחקרים שבוצעו לאחרונה לאחר מגפת הקורונה הדגימו כי גם דילוג על מספר מצומצם של הזרקות – הוביל להידרדרות הראייה והתקדמות מהירה יותר לעיוורון אצל המאובחנים.
בנייר עמדה של האיגוד האמריקאי לרפואת העין (AAO) מפברואר 2014, נקבע כי נכון להיום "יש להימנע מבדיקות גנטיות שגרתיות למחלות עיניים עם מורכבות גנטית כמו ניוון מקולרי גילי (וכן סוגים מסוימים של גלאוקומה) עד שטיפול ספציפי או אסטרטגיות טיפוליות יוכיחו יעילות למטופלים עם גנוטיפ ספציפי". לפי עמדת האיגוד, בשלב הנוכחי ביצוע בדיקות גנטיות למטופלים צריך להתבצע במסגרת מחקרית בלבד.
ההתקדמות בפיתוח טיפולים גנטיים לניוון מקולרי גילי תדרוש חשיבה מחדש על הצורך בבדיקות גנטיות למאובחנים במחלה ואף לקרוביהם של חולים במחלה.
פיתוח טיפולים גנטיים לניוון מקולרי
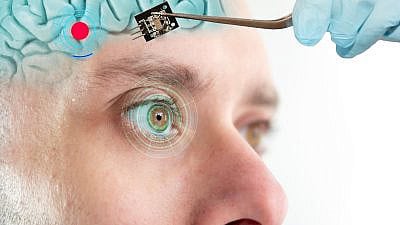
מספר חברות תרופות וביוטכנולוגיה נמצאות כבר היום בשלבי פיתוח של טיפולים גנטיים לניוון מקולרי, שמטרתם "לנטרל" גנים שזוהו כקשורים בהתפתחות והתקדמות של ניוון מקולרי – בניסיון למנוע את המחלה או לקדם את ריפויה. הטיפולים החדשים מבקשים להשפיע בעיקר על גנים הקשורים בהתפתחות כלי דם פתולוגיים שמאפיינים את השלב הרטוב של ניוון מקולרי גילי וכן גנים שקשורים בפעילות דלקתית בעין שמאיצה את התקדמות המחלה.
מטרת הטיפול הגנטי היא לספק טיפול חד פעמי שיסייע לעין לייצר בעצמה תרופה כנגד כלי דם פתולוגיים שמתפתחים ברשתית בשלב הרטוב של המחלה, כחלופה להזרקות התוך עיניות הקיימות. בין השאר נבדקת כיום שיטה כוללת הזרקה של הטיפול הגני מתחת לרשתית במסגרת הליך כירורגי; ולצדה נבחנת הזרקה של הטיפול הגנטי לתוך העין, בדומה לטיפול השגרתי בהזרקות תוך עיניות. למרות ההבטחה שטמונה בטיפול הגני, יעילותו לטווח ארוך עדיין אינה ידועה. טיפול כזה גם צפוי להיות יקר מאוד, וייתכן שלא יתאים לכלל המאובחנים עם ניוון מקולרי רטוב.
הטיפולים הגנטיים המפותחים לניוון מקולרי זוכים לרוח גבית לאור ההתקדמות בתחום הטיפולים הגנטיים בתחום רפואת העין. בדצמבר 2017 אישר מינהל המזון והתרופות האמריקאי (ה-FDA) לראשונה טיפול גנטי פורץ דרך בתרופה לוקסטורנה (Luxturna), שמיועדת לילדים עם 'רטיניטיס פיגמנטוזה' שנגרמת על רקע שינוי בגן RPE65, ומובילה אף היא לניוון הדרגתי של הרשתית עד לעיוורון. התרופה מחדירה לגוף בזריקה חד פעמית לתוך העין גן חדש ותקין של RPE65 על גבי וירוס, באופן שמאפשר מניעת עיוורון וריפוי מהמחלה. בינואר 2020 התרופה אף נכנסה לסל הבריאות הממלכתי בישראל.
אחד הטיפולים הגנטיים שנחקרים כיום מכונה ABBV-RGX-314, והוא עושה שימוש בווירוס לא מזיק מסוג 'אדנו וירוס' שמשמש נשא המחדיר לעין באופן חד פעמי קוד גנטי חדש המוביל לייצור מתמשך של מקטע של נוגדן הנקשר לחלבון VEGF-A וחוסם את פעילותו. כשנחסמת פעילות החלבון, שבמצב של ניוון מקולרי מתקדם מעודד היווצרות כלי דם פתולוגיים ודליפה ברשתית, פעילות זו מדוכאת, וכך נבלמת התקדמות המחלה ללא צורך בהזרקות תוך עיניות שמפעילות גם כן את המנגנון הביולוגי שחוסם את החלבון VEGF. באפריל 2024 דווח בכתב עת Lancet כי הפיתוח עבר את שלב מחקר הבטיחות – שלב 1 מתוך שלושת שלבי הפיתוח של תרופות חדשות – מבלי לעורר תגובות אימוניות משמעותיות. באוקטובר 2024 דיווחה החברה על תוצאות ממחקר של שלב 2, שהדגימו את יכולת הטיפול להפחית את הצורך בהזרקות תוך עיניות לחולים עם ניוון מקולרי רטוב דו־צדדי, שקיבלו את הטיפול הגני בעין השנייה לאחר טיפול קודם בעין הראשונה.
לצד טיפול זה, מצויים בשלבי מחקר מתקדמים טיפולים גנטיים בתרופות המכונות SAR402663 ,4D-150 ו-ADVM-022, אשר באופן דומה מבקשים להחליף את הצורך בהזרקות תוך עיניות באמצעות טיפול גנטי חד פעמי שחוסם את המסלול הוביל ליצירת כלי דם מזיקים ברשתית העין. הטיפול SAR402663 קיבל בספטמבר 2025 אישור של מינהל המזון והתרופות האמריקאי (ה-FDA) לפיתוח מזורז. טיפולים פורצי דרך אלה נבחנים הן לניוון מקולרי והן למחלות רשתית נוספות שמתאפיינות בצמיחת כלי דם חדשים ברשתית, למשל רטינופתיה סוכרתית.
מספר טיפולים גנטיים המפותחים בשנים האחרונות מכוונים כנגד ווריאנטים בקבוצת הגנים של מערכת המשלים, ונבדקים להשפעתם על סיבוך מסוג אטרופיה גאוגרפית של ניוון מקולרי יבש. אחד מהם הוא התרופה GEM103, שקיבלה אף היא בינואר 2021 את אישור מינהל התרופות האמריקאי לפיתוח מואץ. במסגרת טיפול זה מוזרק לעין גן CHF תקין, לתאי המקולה, באופן שמאפשר להן לייצר חלבוני CHF תקינים המגנים מפני דלקתיות והחמרת התהליך הניווני בעין. באפריל 2022 פורסם בעיתונות המדעית כי הפיתוח עבר בהצלחה את שלב מחקר הבטיחות – שלב 1. יש לציין כי טיפול זה מצריך הזרקות חוזרות מדי חודש.
לצד זאת נחקר טיפול גנטי בשם OCU410 המחדיר לגוף קולטן ייעודי בשם RORA שמווסת מסלולים חיוניים לתפקוד תקין של רשתית העין, לרבות פעילות מערכת המשלים, עקה חמצונית, דלקתיות ומטבוליזם השומנים, באופן המאפשר לבלום את תהליך ההתקדמות של אטרופיה גאוגרפית בהזרקה אחת בלבד. בחודשים האחרונים דווח על תוצאות חיוביות בשלב 2 של הפיתוח, וההערכות כי השלב השלישי האחרון בניסויים הקליניים לאישור התרופה יחל במהלך 2026. בשנים האחרונות נחקר גם טיפול גנטי דומה בשם GT005 המבקש להזריק לעין בהזרקה חד פעמית את הגן CFI הדומה בתפקודו לגן CHF, במטרה "לתקן" את הפגיעה בתפקוד מערכת המשלים שנקשרה להתפתחות והתקדמות של אטרופיה גאוגרפית, אולם בספטמבר 2023 דווח כי הופסק פיתוח התרופה על רקע תוצאות שאינן משביעות רצון.
מיון גנטי טרום השרשתי
מהרגע שאובחנו שינויים גנטיים שנקשרו לניוון מקולרי גילי, תיאורטית נפתחה האפשרות לביצוע מיון גנטי טרום השרשתי בשיטות PGT ו-PGT-A – כדי להבטיח הולדה של עוברים שאינם נושאים וריאנטים גנטיים אלה. טיפול זה כרוך בצורך בטיפולי הפריה חוץ גופית.
מבחינה פרקטית כבר מבוצעים טיפולים לאיתור מוטציות גנטיות שנקשרו למחלות מורכבות בביציות מופרות, אך כיום לא נעשה שימוש בטכנולוגית המיון הגנטי בניוון מקולרי, מאחר ומדובר במחלה המפתחת בגיל המבוגר בשילוב של וריאנטים גנטיים ואורח חיים, כך שגם לאחר השקעה באיתור וריאנטים גנטיים פגועים ובחירת עוברים בריאים לכאורה להפריה – קשה לקבוע האם פעילות זו אכן תלווה בירידה בסיכון להתפתחות המחלה מגיל 50 ומעלה.
בינתיים: נצמדים לאורח חיים בריא
בעוד שהתובנות על ההשפעות הגנטיות על ניוון מקולרי גילי מוסיפות להתברר, ולצד מחקרים שמתוכננים ומבוצעים במטרה לפתח טיפולים גנטיים למחלה – נכון להיום מומלץ לכל מי שאובחנו במשפחתו הביולוגית חולים בניוון מקולרי גילי להקפיד על צעדים מניעתיים הקשורים באורח חיים בריא, שהוכחו כמפחיתים את הסיכון להתפתחות של ניוון מקולרי גילי ולאבחון המחלה בשלבים מוקדמים כדי לעכב את התקדמותה:
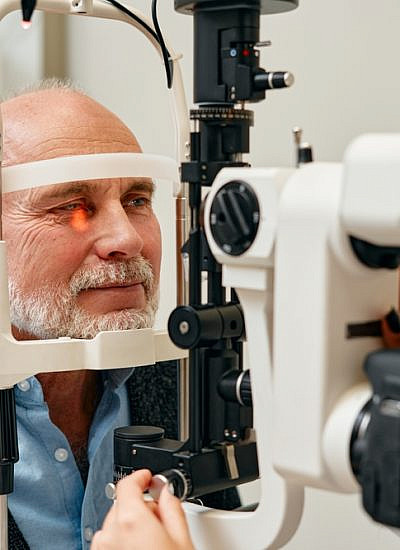
- הגעה לבדיקות שגרתיות אצל רופאי עיניים. המלצה הבסיסית כיום בתחום רפואת העיניים היא לפנות לרופא עיניים בכל מקרה של תסמינים שמעידים על הפרעה אפשרית בראייה. ההמלצה המקובלת באוכלוסייה הכללית היא לבצע בדיקות עיניים מקיפות למחלות עיניים מגיל 50 עד גיל 65 אחת ל-4-3 שנים, ומגיל 65 ומעלה אחת לשנה-שנתיים, וכן בדיקות אחת לשנה למאובחנים עם סוכרת, מחלות עיניים, לאחר שימוש ממושך בסטרואידים או במקרה של מחלת עיניים במשפחה.
- לאור הקשר הגנטי של ניוון מקולרי, לקרוביהם של מי שאובחנו עם ניוון מקולרי גילי יש חשיבות רבה במיוחד לביצוע בדיקות עיניים סדירות אחת לשנה לאחר גיל 50 לאיתור המחלה בשלבים מוקדמים.
- מומלץ להקפיד על תזונה מאוזנת שאינה מכילה כמויות גבוהות של שומן רווי וסוכר ועשירה בפירות וירקות. מספר ויטמינים, מינרלים ונוגדי חמצון הוכחו ביכולתם לעכב התקדמות של ניוון מקולרי ואלה כלולים בתוסף תזונה ייעודי המומלץ למאובחנים.
- מומלצת פעילות גופנית סדירה שביכולתה לעכב את התקדמות המחלה.
- מומלצת גמילה מעישון סיגריות – אשר הוכח כגורם בר המניעה הראשון במעלה לניוון מקולרי גילי.
- יעוץ מקצועי: ד"ר אור שמואלי הוא רופא במחלקת עיניים במרכז הרפואי הדסה השוהה בפלושיפ בתחום מחלות רשתית במחלקת העיניים של בתי החולים Toronto Western ו-Sunnybrook של אוניברסיטת טורונטו בקנדה, מנהל בקהילת ניוון מקולרי גילי באתר "כמוני"
עדכון אחרון: פברואר 2026