מתחם אפילפסיה
פרקינסון – כל מה שחשוב לדעת
מהי מחלת הפרקינסון ומה תסמיניה האופייניים? מהם גורמי הסיכון להתפתחותה? איך מאבחנים פרקינסון? ואילו טיפולים עיקריים יוכלו להועיל?

פרקינסון (Parkinson) היא מחלה כרונית פרוגרסיבית שמשפיעה על המוח ועל אזורים בגוף שנשלטים על ידי מערכת העצבים המרכזית.
התסמינים של פרקינסון לרוב מתקדמים בקצב איטי. לרוב הביטוי למחלה מופיע תחילה כרעד קל ביד אחת בלבד, והיא עלולה עם הזמן לגרום לרעידות, נוקשות והאטה בתנועתיות באזורים שונים בגוף, קשיים בדיבור וסיבוכים נוספים.
למרות שאין כיום בנמצא טיפול שמאפשר לרפא פרקינסון, תרופות מקבוצות שונות עשויות לסייע לשיפור משמעותי של התסמינים. במצבים קשים יומלץ לעתים גם על ניתוח נוירוכירורגי להשתלת קוצב מוח למיתון התסמינים.
בכתבה זו נפרט על:
התסמינים של פרקינסון
מחלת הפרקינסון עשויה להתבטא באופן שונה ממטופל למטופל במנעד רחב של תסמינים.
בשלב הראשון, התסמינים עשויים להיות קלים ביותר, ולעתים אף אינם מורגשים. הביטוי הראשון מערב לרוב חולשה בצד אחד של הגוף וגם עם התקדמות המחלה – כשזו משפיעה על שני צידי הגוף, צד אחד לרוב חמור יותר.
בין התסמינים האפשריים של פרקינסון נמנים:
- רעד: רעד קצבי (Tremor) בזמן מנוחה לרוב מתחיל באחת הגפיים – ביד או באצבעות. באחד הביטויים של הרעד נדמה שהמטופל/ת מגלגל/ת כדור זעיר בין האצבעות או סופר כסף – מצב המכונה ברפואה Pill-rolling tremor. הרעד נוטה להתמתן בעת ביצוע משימות. לפי מחקר אמריקאי שפורסם בדצמבר 2020, בהתבסס על מדגם בהשתתפות מעל לאלף מאובחנים עם פרקינסון, על רעידות במנוחה מעידים מעל למחציתם (58.2%) ועל רעידות במהלך פעילות מעידים מעל לשליש (39%) מהמטופלים.
- תנועות איטיות: מחלת הפרקינסון מובילה עם הזמן להאטה בביצוע פעולות כתוצאה מכך ששרירי הגוף פועלים "בהילוך איטי" ובקואורדינציה ירודה, מצב המכונה ברפואה 'ברדיקינזיה' (Bradykinesia). במצב זה המטופלים נוהגים להתהלך באיטיות רבה יותר, כשהצעדים נעשים קצרים יותר, ולעתים מתפתחת "גרירת רגליים", והם עשויים להתקשות בפעולות מסוימות, למשל לקום מהכיסא. מצב נוסף שמאפיין פרקינסון בשלבים מתקדמים יותר קרוי 'קיפאון הליכה' (Freezing of gait), ומתבטא בחוסר יכולת פתאומית להמשיך ולצעוד עם אחת הרגליים קדימה למרות הרצון להמשיך וללכת.
- נוקשות שרירים: פרקינסון עשויה להתבטא בנוקשות שרירים בכל אחד מאזורי הגוף. תסמין זה עשוי להתפתח לכדי מגבלות תנועתיות ובכאבי שרירים.
- חוסר שיווי משקל: פרקינסון עשוי לפגוע ביציבה ובשיווי המשקל, ומעלה את הסיכון לנפילות.
- אובדן תנועות אוטומטיות: פרקינסון נוטה להתבטא בירידה ביכולת לבצע תנועות אוטומטיות שאינן דורשות מודעות, למשל מצמוץ בעפעפיים, חיוך והנעת הזרועות תוך כדי הליכה.
- שינויים בדיבור: פרקינסון עשוי עם הזמן להוביל לשינויים בטון הדיבור, ולדיבור רך יותר, איטי והססני יותר, או לחילופין לדיבור מהיר יותר. טון הדיבור נוטה להיות יותר מונוטוני, ולרוב ניכר בו דפוס שחוזר על עצמו, ללא גמישות מתבקשת של דיבור בדפוסים משתנים.
- שינויים בכתיבה: פרקינסון עשוי לפגוע עם הזמן ביכולת הכתיבה, והכתב עשוי להפוך לקטן יותר ופחות ברור – על רקע הרעד בידיים.
במקרה שהתפתחו תסמינים שמעוררים חשד לפרקינסון – חשוב לבקש הפניה לרופא נוירולוג לצורך אבחון וכן שלילה של מצבים רפואיים אחרים שעשויים להתבטא בתסמינים דומים.
השכיחות של פרקינסון
פרקינסון היא מחלה נוירולוגית שאינה נדירה במיוחד, ושכיחותה נאמדת בכ-10 מיליון איש ברחבי העולם, פחות מאחוז באוכלוסייה. מחקר שמבוסס על מחקרים בספרות הרפואית והוצג בכנס בספטמבר 2020 העריך כי בעולם חיים 9.4 מיליון איש עם פרקינסון, ובארה"ב לבדה כ-930 אלף חולים. עד שנת 2040 צפוי מספר החולים ברחבי הגלובוס להאמיר לכ-14.2 מיליון איש.
בישראל מוערך כי חיים כ-35 אלף חולי פרקינסון.
לפי מחקר נרחב שמבוסס על נתוני כלל החולים בקופת חולים מכבי, שממצאיו פורסמו בשנת 2011 בכתב העת Journal of Parkison's Disease, שיעורי התחלואה בארץ בשנים 2000 עד 2007 עמדו על 170 עד 256 לכל מאה אלף איש. במחקר שפורסם עוד בחורף 2002 בכתב העת Neuroepidemiology, הוערך כי מפתחים את המחלה כ-0.24% מתושבי הקיבוצים, בהם קרוב לאחוז אחד (0.94%) מהקיבוצניקים מעל גיל 60 וכן 0.33% מהקיבוצניקים מעל גיל 40.
יש עדויות ולפיהן שיעורי התחלואה בפרקינסון בישראל כפולים בהשוואה לשיעורים במדינות אחרות – על רקע סיכון גנטי גבוה יותר למחלה באוכלוסייה היהודית אשכנזית (קראו בהרחבה בהמשך הכתבה).
מחקרים מזהים בשנים האחרונות עלייה בהיקף התחלואה בפרקינסון. במחקר שסקר את שכיחותה בעולם, שפורסם בנובמבר 2018 בכתב העת Lancet Neurology, נמצא כי משנת 1990 עד 2016 גדלה שכיחות המחלה ב-21.7%. לדברי ד"ר גלעד יהלום, מנהל היחידה להפרעות תנועה במרכז הרפואי שערי צדק ויו"ר החברה הישראלית להפרעות תנועה, "פרקינסון היא מחלה של הגיל המבוגר, וככל שתוחלת החיים עולה ויש הזדקנות של האוכלוסייה, יש עלייה במחלות אופייניות כמו פרקינסון ודמנציה".
סיבות וגורמי סיכון לפרקינסון
במחלת הפרקינסון פעילות תאי עצב במוח (הנוירונים) נפגעת בהדרגה, כאשר התסמינים מופיעים על רקע הרס או ניוון של תאים שמייצרים את המוליך העצבי דופמין (Dopamine) וכתוצאה מירידה ברמות הדופמין במוח.
עם השנים נמצא כי חולי פרקינסון מאבדים מעל ל-80% מהתאים מייצרי הדופמין באזור החומר השחור (Substantia Nigra) במוח.
לצד הפגיעה בייצור הדופמין במוח, מחקרים מזהים שינויים מבניים ותפקודיים נוספים שעשויים להתפתח במוחם של אנשים עם פרקינסון מסיבות שאינן ברורות לאשורן:
- נוכחות של גופיפי לואי/ לוי: מצבורים של חלקיקים כדוריים מיקרוסקופיים המכונים ברפואה 'גופיפי לואי/ לוי' (Lewy bodies) נצפים בתאי מוח של אנשים עם פרקינסון. כיום ההבנה במחקר כי גופיפים אלה עשויים לספק הסבר לסיבה שמובילה להתפתחות המחלה.
- אלפא-סינוקלאין: גופיפי לואי/לוי מורכבים מחומרים שונים, אך מדענים מאמינים כי אחד החומרים החשובים בהתפתחות פרקינסון הוא חלבון בשם 'אלפא-סינוקלאין' (α synuclein). מחקרים זיהו חלבון זה בדגימות נוזל חוט שדרה של אנשים שפיתחו בהמשך פרקינסון.
הסיבה לפגיעה בתאים מייצרי דופמין במוח אינה ידועה, אולם מחקרים מצביעים על מספר גורמי סיכון שעשויים להיות מעורבים בכך, בנפרד או במשולב:
- גנטיקה: חוקרים זיהו ברבות השנים סיכון גנטי לפרקינסון ומשפחות אצלן במחלה עוברת בתורשה. כמו כן, עבודות זיהו שינויים ספציפיים בגנים שנקשרו להתפתחות המחלה, אם כי ההנחה כי הסיכון הגנטי למחלה משולב גם בגורמי סיכון סביבתיים. עד כה תועדו מספר מוטציות גנטיות שכיחות באוכלוסייה האשכנזית שמעלות את הסיכון לפרקינסון. בינואר 2006 דיווחו חוקרים ישראלים בכתב העת New England Journal of Medicine על מחקר שנערך בבית החולים "בית ישראל" בניו יורק במסגרתו זוהתה מוטציה המסומנת באותיות G2019S בגן המסומן באותיות LRRK2, אשר שכיחה במיוחד באוכלוסייה יהודית-אשכנזית, וקיומה מעלה את הסיכון לפרקינסון.
- חשיפה למזהמים: מספר חומרים מזהמים נקשרו במחקרים לעלייה בסיכון להתפתחות פרקינסון. מספר מחקרים, שחלקם בוצעו גם בישראל בקרב עובדי ענף החקלאות – מצאו כי חשיפה מסוכנת ומתמשכת לחומרי הדברה מעלה בעשרות אחוזים את הסיכון לפתח פרקינסון. מחקר אמריקאי שפורסם בנובמבר 2023 בכתב העת Neurology מצא כי אזורים בארה"ב ניתנים להבחנה בשיעורי התחלואה בפרקינסון בהתאם לרמות החשיפה לחלקיקי זיהום אוויר שמסוגלים לחדור את דרכי הנשימה.
מחקרים מצביעים על מספר גורמי סיכון אפשריים נוספים להתפתחות פרקינסון:
- גיל: הסיכון לפרקינסון גדל עם העלייה בגיל, ולרוב העלייה בסיכון מתחילה בגיל העמידה. פרקינסון אצל צעירים נחשב למחלה נדירה למדי, שמתפתחת בעיקר על רקע הגנטי. רוב החולים בפרקינסון מאובחנים בגילי 60 ומעלה.
- מין: לגברים סיכון גבוה יותר להתפתחות פרקינסון, בהשוואה לנשים. במחקר מישראל שמבוסס על נתוני המבוטחים בקופת חולים מכבי, התברר כי מעל גיל 50 שכיחות הפרקינסון הייתה גבוהה ב-38% יותר בקרב גברים, בהשוואה לנשים.

חומרי הדברה הם גורמי סיכון סביבתיים מוכחים לפרקינסון (צילום: Shutterstock)
סיבוכים של פרקינסון
מחלת פרקינסון עשויה להיות מלווה בסיבוכים רפואיים נוספים. סיבוכים אלה מכונים לעתים 'תסמינים לא מוטוריים' (Non-Motor Symptoms), ולעתים הם אלו שמהווים את עיקר הבעיה עבור המטופלים, אפילו יותר מהתסמינים המוטוריים. לחלק מהתסמינים ניתן להציע טיפולים תרופתיים סימפטומטיים, לצד הטיפול במחלה עצמה.
- ירידה קוגניטיבית: פרקינסון מלווה במקרים רבים בפגיעה קוגניטיבית, ולעתים המחלה מאובחנת במקביל למחלות דמנציה כמו אלצהיימר. לפי הערכות, עד 70% מהאנשים עם פרקינסון צפויים לפתח הפרעות שמאופיינות בדמנציה עם התקדמות המחלה. בעיות קוגניטיביות לרוב מופיעות בשלבים מתקדמים יותר של פרקינסון, ולרוב אינם ניתנים לטיפול תרופתי, אם כי כיום יש טיפולים שביכולתם להאט/ לעכב את ההחמרה ביכולות קוגניטיביות.
- מצוקה נפשית: לאנשים עם פרקינסון סיכון גבוה יותר להתמודד עם מצוקה נפשית ודיכאון, לעתים כבר בשלבים הראשונים למחלה. במקרים רבים טיפול תרופתי בנוגדי דיכאון מסייע לשיפור איכות חייהם של החולים. פרקינסון עשויה גם להיות מלווה בשינויים רגשיים, כגון חרדות ואובדן מוטיבציה. יש גם מחקרים שטוענים לקשר מעגלי בין דיכאון לעלייה בסיכון להתפתחות פרקינסון. ככל הנראה, הקשר בין התופעות מוסבר בשינויים מבניים במוח, שינויים בפעילותם של מוליכים עצביים מסוימים ועלייה בדלקתיות ובחלבונים נוספים במוח (גורמים נוירוטרופיים). לפי מאמר בנושא שפורסם בדצמבר 2011 בכתב העת Nature Reviews Neurology, נקבע כי בקרב המאובחנים עם פרקינסון, כשליש (35%) מתמודדים עם דיכאון, לרוב לתקופה ממושכת.
- הפרעות בליעה: מחלת פרקינסון עשויה להוביל עם הזמן לקשיים בבליעה – הקרויים בעגה הרפואית 'דיספגיה' (Dysphagia), לרבות הצטברות רוק בפה בגלל קשיי בליעה, המובילה להזלת ריר. לפי מטה אנליזה מסין שפורסמה באוקטובר 2022 בכתב העת Frontiers in Neurology, מעל לשליש מהמאובחנים עם פרקינסון (36.9%) מפתחים הפרעות בליעה.
- הפרעות לעיסה: בשלבים מתקדמים של פרקינסון, המחלה עשויה לפגוע בשרירי הפה ולהוביל גם להפרעות בלעיסת מזון, מה שעשוי להוביל למצבים של חנק, פגיעה ביכולות אכילה וכתוצאה מכך גם לפגיעה בצריכת מרכיבים תזונתיים חיוניים וסיכון לתת תזונה.
- הפרעות שינה ועייפות: אנשים רבים עם פרקינסון מדווחים על הפרעות שינה, לרבות יקיצות מרובות באמצע הלילה, קימה בשעה מוקדמת בבוקר ועייפות קשה שמלווה בהירדמות במשך היום. מטה אנליזה בנושא מאיטליה, שפורסמה באפריל 2023 בכתב העת Sleep Medicine Reviews, מצאה כי לקרוב ממחצית מהאנשים עם פרקינסון (46%) יש נטייה להפרעות שינה, ומעל לשליש (35%) מתמודדים עם עייפות חמורה במשך היום, בעיקר מבוגרים, וחולים לתקפה ממושכת יותר ועם רמת אוטונומיה נמוכה יותר. יש חולי פרקינסון שמפתחים הפרעת התנהגות בשנת REM שמתבטאת בהתנהגות חריגה במהלך שנת החלום המאופיינת בתנועות עיניים חריגות, כשהמטופל נוטה להתנהג בהתאם למה שהוא חולם ולעתים מפגין התנהגות אלימה לא מודעת לסביבה. טיפול תרופתי בכדורי שינה עשוי לסייע לשיפור איכות השינה.
- הפרעות בשלפוחית השתן: מחלת פרקינסון עשויה להיות מלווה במחלות של שלפוחית השתן, ובהן אי שליטה במתן שתן וקשיים במתן שתן. מטה אנליזה בנושא מסין, שפורסמה בספטמבר 2022 בכתב העת Frontiers in Aging Neuroscience זיהתה תלונות של בעיות אגירה בשלפוחית השתן בקרב מעל למחצית (54%) מהמתמודדים עם פרקינסון ודליפת שתן אצל קרוב לשליש (30%) מהמאובחנים. טיפול תרופתי סימפטומטי עשוי להקל בסיבוכים אלה.
- עצירות: רבים מהסובלים מפרקינסון מעידים על עצירות, בעיקר כתוצאה מהאטה בפעילות מערכת העיכול. מטה אנליזה מסין, שפורסמה בפברואר 2023 בכתב העת European Neurology, מצאה כי לאנשים עם פרקינסון סיכוי גבוה פי 2.36 לסבול מעצירות כרונית, בהשוואה לאוכלוסייה הכללית. טיפול תרופתי סימפטומטי עשוי להקל בסיבוך זה.
- שינויים בלחץ הדם: פרקינסון עשוי להתבטא בשינויים פתאומיים בלחץ הדם ובתחושת סחרחורת בעמידה על רקע ירידה פתאומית בלחץ הדם – מצב רפואי הקרוי 'תת לחץ דם תנוחתי' (Orthostatic Hypotension).
- הפרעות בחוש ריח: פרקינסון עשוי להיות מלווה בהפרעות בחוש הריח, ובין השאר גם בקושי בזיהוי ריחות שונים ובאבחנה בין ריחות. פגיעה בחוש הריח מופיעה אצל רוב המאובחנים עם פרקינסון כבר בשלבים מוקדמים של המחלה, ולעתים אף משמשת כאמצעי לאבחון המחלה. יש הערכות כי הפגיעה בחוש הריח נגרמת אצל חולי פרקינסון על רקע שינויים בפעילות המוליכים העצביים במוח מסוג תאי עצב כולינרגים וכן הכימיקלים סרוטונין ונוראדרנלין. מחקר אמריקאי מאוניברסיטת פיטסבורג שפורסם בספטמבר 2008 בכתב העת Neuroscience Letters מצא עדות לקשר בין פגיעה בחוש הריח אצל אנשים עם פרקינסון לבין פעילות משובשת של דופמין באזור ההיפוקמפוס שבמוח.
עוד על מחלות שגורמות לפגיעה בחוש הריח
- כאבים: פרקינסון עשויה להיות מלווה בכאבים, לעתים כאב ממוקד באזור מסוים בגוף ולעתים כאבים מפושטים באזורי גוף נרחבים. מטה אנליזה בנושא מקנדה, שפורסמה בשנת 2018 בכתב העת Neuroepidemiology מצאה כי מעל לשני שליש (68%) מהמאובחנים עם פרקינסון מתלוננים על כאבים, אך במחצית מהמקרים (50%) הבעיה לא מטופלת.
- הפרעות בתפקוד המיני: חלק מהאנשים עם פרקינסון מרגישים עם התקדמות המחלה ירידה בחשק המיני ובתפקוד המיני. מטה אנליזה מאיראן, שפורסמה בנובמבר 2023 בכתב העת Journal of Clinical Neuroscience, מצאה כי אבחון בפרקינסון מעלה פי 3.5 את הסיכוי לפגיעה בתפקוד המיני בקרב גברים ונשים כאחד.
מניעת פרקינסון
מאחר והסיבות להתפתחות פרקינסון עוד אינן ידועות לאשורן, אין נכון להיום שיטות מוכחות למנוע פרקינסון. יחד עם זאת, מספר מחקרים מצביעים על שיטות שעשויות להפחית את הסיכון לפתח את המחלה:
- פעילות גופנית: מחקרים מצביעים על כך שפעילות גופנית אירובית עשויה להפחית את הסיכון לפרקינסון. מטה אנליזה מסין, שפורסמה במארס 2021 בכתב העת Annals of Palliative Medicine מצאה כי פעילות אירובית, למשל בהליכה מהירה, ריצה, שחייה או רכיבה על אופניים, מסייעת לשיפור שיווי המשקל והיציבה, אולם לא תמיד עם השפעה משמעותית על תסמינים מוטוריים.
- צריכת קפאין: מספר מחקרים מראים כי אנשים שצורכים קפאין, בין אם בקפה, תה או משקאות קולה, נמצאים בסיכון נמוך יותר לפתח פרקינסון. יש ראיות נוספות כי קפאין עשוי לעכב את התפרצות המחלה והתקדמותה, ושתייני קפה עם פרקינסון נוטים לפתח את המחלה בגילים מאוחרים יותר. גם שתיית תה ירוק נמצאה קשורה בירידה בסיכון לפרקינסון. לפי מטה אנליזה מטאיוואן, שפורסמה ביוני 2020 בכתב העת Nutrients, צריכה קבועה של קפאין מפחיתה ב-21% את הסיכון לפרקינסון, וגם מאטה את קצב התקדמות המחלה. למרות זאת, לא ניתן לקבוע על פי המידע הידוע היום כי קפאין מגן מפני פרקינסון, ואין נכון להיום די מידע כדי לבסס המלצה לשתיית משקאות עם קפאין כאמצעי למניעת המחלה.

קפאין – קשור בירידה בסיכון לפרקינסון (צילום: Shutterstock)
אבחון של פרקינסון
נכון להיום אין בדיקה ספציפית שמאפשרת לאבחן במדויק פרקינסון, ותהליך אבחון המחלה מתבסס על בדיקה קלינית שמתבצעת על ידי נוירולוג, בשילוב ממצאים מבדיקות נלוות.
בבדיקה הקלינית מתבצע בירור להיסטוריה רפואית משפחתית ולתסמינים האופייניים ומתבצעת בדיקה נוירולוגית ופיזית.
במקרים מסוימים, על בסיס הבדיקה הנוירולוגית, יופנו המטופלים לבדיקת הדמיה ייחודית מסוג SPECT שמטרתה לייצר תמונה תלת ממדית על ידי הזרקת מולקולות רדיואקטיביות. בבדיקה ושמה DaT (Dopamine Transporter) מתבצעת סריקה לאיתור חלבוני העברה (טרנספורטרים) של המוליך העצבי דופמין, אשר אחראים להעברתו לתוך התא. כך ניתן לקבל באופן עקיף מידע על רמות הדופמין במוח. חיסרון השיטה שהיא אינה מאפשרת להבחין בין פרקינסון למחלות נוספות שקשורות בפגיעה ברמות הדופמין, ולכן לא נעשה בה שימוש שגרתי בתהליך אבחון המחלה. כמו כן, בישראל הבדיקה יקרה ואינה כלולה בסל הבריאות הממלכתי, ולכן השימוש בה אינו נפוץ.
בתהליך האבחנה ייתכן הצורך בבדיקות דם לשלילת מצבים רפואיים נוספים שעשויים להסביר את התסמינים. כמו כן, לעתים מתבצעות בדיקות הדמיה מסוג MRI, אולטרה-סאונד של המוח או הדמיות PET במטרה לשלול מחלות אחרות. חשוב להדגיש שככלל, בדיקות הדמיה אינן מסייעות רבות לאבחנה של פרקינסון.
כמרכיב נוסף, לצורך אימות האבחנה של פרקינסון נהוג לתת למטופלים תרופה מסוג 'קארבידופה לבודופה' (Carbidopa-Levodopa) כדי לבחון את תגובתם לטיפול. 'לבודופה' היא תרופה שמעלה את רמות הדופמין במוח ואילו 'קארבידופה' הווא חומר פעיל שמעכב את הפירוק של 'לבודופה' וכך מעלה את זמינותו במוח. לרוב נדרש טיפול למספר ימים כדי לבחון האם חל שיפור במצב המטופל, וככל שמורגש שיפור כזה – ניתן בכך אישוש לאבחנה של פרקינסון.
מאחר ואין בדיקה ספציפית לאבחון פרקינסון – לעתים חולף זמן עד לאבחנה הסופית במחלה, ויש מצבים בהם נדרשים מספר מעקבים אצל נוירולוגים לצורך הערכה מלאה והשלמת תהליך האבחון.
חשוב לציין כי בקהילה הרפואית והמדעית מתבצעות בשנים האחרונות ניסיונות לאיתור שיטה מתקדמת יותר לאבחון של פרקינסון בשלבים מוקדמים. אחת הבדיקות שכבר נמצאת בשלבי מחקר מתקדמים קרויה בדיקת αSyn-SAA (קיצור של alpha-synuclein Seed Amplification Assay) בודקת את רמות החלבון 'אלפא סינוקלאין' המצוי בגופיפי לואי בנוזל חוט השדרה, ובמחקר שפורסם במאי 2023 בכתב העת Lancet Neurology נמצא כי ביכולתה לזהות ברמת דיוק של 87.7% פרקינסון. מחקרים נרחבים יותר בוחנים כיום את יעילות הבדיקה, ויש תקווה בקרב מדענים כי ניתן יהיה בעתיד גם לפתח בדיקה לאבחון פרקינסון על סמך בדיקת דם וללא צורך בדיקור מותני לצורך הוצאת דגימה של נוזל חוט השדרה.
הטיפולים לפרקינסון
מחלת הפרקינסון איננה ניתנת לריפוי, אולם יש כיום כלים טיפוליים שמאפשרים לשלוט בתסמינים ולעתים לעכב את התקדמותה ולשפר את איכות חיי המאובחנים. הטיפולים העיקריים כוללים תרופות, ובמקרים קשים יותר – טיפולים פולשניים ובהם ניתוחים כירורגים.
תרופות לפרקינסון
תרופות מסייעות למתן את התסמינים האופייניים של פרקינסון, ובכללם בעיות תנועה, הליכה ורעידות.
מטרת התרופות המרכזית היא העלאה ברמות הדופמין במוח. לא ניתן לתת למטופלים דופמין באופן ישיר, מאחר והוא אינו חודר את מחסום הדם-מוח. לכן נדרשת העלאת רמות הדופמין בשיטות עקיפות. יעילות התרופות לפרקינסון עשויה להיות מוצלחת ביותר בשלבים הראשונים, אולם לרוב עם הזמן השפעת התרופות נחלשת, ותסמיני המחלה עשויים להתגבר.
לדברי ד"ר יהלום, "התאמת תמהיל הטיפול התרופתי נעשית בכל מקרה לגופו, בהתאם לחומרת התסמינים ולנתונים נוספים. אם התסמינים בולטים, נהוג להתחיל את הטיפול בשילוב 'קארבידופה-לבודופה', ואם התסמינים קלים – נהוג בשלב הראשון לטפל בתרופות מקבוצת מעכבי MAO-B כמו רסג'ילין ואזילקט, שייתכן ויש להן השפעה שמעכבת במעט את התקדמות ההמחלה, והן מלוות בתופעות לוואי פחות משמעותיות".
התרופות בשימוש נרחב לפרקינסון כוללות:
- קארבידופה-לבודופה
התרופה קארבידופה-לבודופה (Carbidopa-Levodopa) שכוללת 'לבודופה' – כימיקל טבעי שחודר למוח והופך לדופמין, לצד 'קארבידופה' – חומר נוסף שמונע את פירוק הלבודופה בגוף ומעלה את זמינותו במוח. התרופה משווקת בישראל בשמות דואודופה, דופיקר, לסיגון, סטאלבו, סינמט ופרודואודופה. התרופה ניתנת בכדורים בשחרור מושהה. בדצמבר 2018 אושרה בארה"ב התרופה בשאיפה לאף בשם אינבריג'ה, אולם זו עדיין אינה זמינה בארץ באופן מלא. תרופה זו עשויה להועיל במקרים בהם התרופה בכדורים מפסיקה להשפיע במהלך היום. לחולים בשלבים מתקדמים, התרופה משווקת גם ג'ל בשם דואודופה, שניתן באמצעות משאבה מיוחדת שמחוברת לגוף בניתוח תחת אשפוז, בהזלפה רציפה ישירות למעי הדק.
קארבידופה-לבודופה כלולה בסל הבריאות הממלכתי מקרים של פרקינסון בלתי נשלט, כשהטיפול בכדורים כבר לא עוזר, כשאבדה היכולת לבלוע כדורים וכן במקרים בהם המחלה מלווה בתסמינים משמעותיים הקשורים בתנועה.
תופעות הלוואי השכיחות של קארבידופה-לבודופה כוללות בחילות וסחרחורות ותת לחץ דם תנוחתי. עם השנים עשויה להתפתח תופעת ללוואי שמתבטאת בשחיקת יעילות הטיפול המכונה On-Off Phenomenon או Wearing Off. התופעה מתבטאת בהחמרה בתסמיני הפרקינסון מספר שעות לאחר נטילת התרופה. תופעת לוואי אופיינית נוספת כוללת תנועות שרירים בלתי רצוניות – ומכונה ברפואה 'דיסקינזיה' (Dyskinesia), וזו דורשת לעתים התאמה של המינונים או של מועדי הנטילה. לחולים עם פרקינסון בשלב מתקדם מומלץ ליטול את התרופה על קיבה ריקה, בהתאם להנחיות הרופאים המטפלים.
- מעכבי MAO-B
תרופות בקבוצת מעכבי MAO-B מעכבות את פעילותו של האנזים MAOB שמפרק את המוליך העצבי דופמין, ובכך משפיעות על עלייה בריכוז הדופמין במוח. בקבוצה זו נכללות התרופות המכילות את החומרים הפעילים רסג'ילין, רסג'ילין מזילאט (אזילקט), סלג'ילין וספינאמיד. התרופה סלג'ילין הניתנת עם לבודופה מסייעת לעתים למתן את הירידה ביעילות התרופה שמתרחשת עם הזמן. יש ראיות שמצביעות על כך שתרופות מקבוצה זו עשויות לעכב התקדמות של פרקינסון בשלבים הראשונים, אם כי הנושא עדיין נתון בוויכוח בקהילה המדעית-רפואית.
תופעות הלוואי של התרופות מקבוצה זו כוללות כאבי ראש, בחילות ונדודי שינה (אינסומניה), וכן הזיות – כשהיא ניתנת בשילוב לבודופה. תרופות מקבוצה זו גם לרוב לא ניתנות למטופלים בתרופות לכאבים ובנוגדי דיכאון עקב חשש מפני תגובות בין תרופתיות.
- אגוניסטים לדופמין
בהבדל מלבודופה, 'אגוניסטים לדופמין' מהווים קבוצת תרופות שלא הופכות לדופמין, אולם "מחקות" את פעולות הדופמין במוח. תרופות אלו אינן נחשבות ליעילות כמו לבודופה, אולם הן מועילות לרוב לזמן רב יותר, ועשויות גם לשמש טיפול משלים ללבודופה כדי למתן את הירידה ביעילות התרופה שמתרחשת עם הזמן. בקבוצה זו נכללות התרופות עם החומרים הפעילים פרמיפקסול – המשמשת גם לטיפול בתסמונת הרגליים חסרות המנוחה וניתנת בטבליות; רוטיגוטין המשווק במדבקות לעור; ואפומורפין שניתן בהזרקה תת עורית באמצעות משאבה ומיועד למצבים של פרקינסון שאינו נשלט באמצעות תרופות הלבודופה.
תופעות הלוואי של אגוניסטים לדופמין עשויות לכלול הזיות, ישנוניות והתנהגות קומפולסיבית, לרבות נטייה להתמכרויות, התקפי זלילה והיפר-סקסואליות.
- מעכבי COMT
תרופות בקבוצה זו מעכבות את פעילות האנזים COMT שמשמש אף הוא לפירוק של המוליך העצבי דופמין, ובכך הן משפיעות על עלייה בריכוז הדופמין במוח. בקבוצה זו התרופות עם החומרים הפעילים אנטקפון ואופיקאפון.
תופעות הלוואי של תרופות אלה כוללות תנועות בלתי רצוניות (דיסקינזיה), לרוב כתוצאה מהעצמת השפעת התרופה לבודופה, וכן שלשולים, בחילות והקאות. תרופה נוספת בקבוצה מכילה את החומר הפעיל טולקפון, אך לאחרונה היא מצויה בשימוש מועט יחסית עקב סיכון לפגיעה בכבד.
- אנטיכולינרגים
תרופות מקבוצת האנטיכולינרגים היו בעבר בשימוש נרחב לטיפול ברעד על רקע פרקינסון, בעיקר לפני עידן הלבודופה, וכיום השימוש בהן ניתן בעיקר כטיפול ייעודי לתסמיני הרעד. אנטיכולינרגים מהווים קבוצת תרופות שחוסמות את פעילות המוליך העצבי אצטילכולין במערכת העצבים המרכזית וההיקפית. בקבוצה זו תרופות המכילות את החומרים הפעילים בנזטרופין וטריהקסיפנידין.
בין תופעות הלוואי של התרופות: הפרעות בזיכרון, בלבול, הזיות, עצירות, יובש בפה ופגיעה במתן שתן.
- אנטגוניסטים לאנזים NMDA
בקבוצת האנטגוניסטים לאנזים NMDA כלולה התרופה אמנטדין שניתנת לעתים לבדה למיתון תסמינים של פרקינסון, מותאמת בשילוב עם לבודופה כדי לטפל בתופעת לוואי של לבודופה המבטאת בתנועות בלתי רצוניות (דיסקינזיה).
לדברי ד"ר יהלום, "תרופה זו ניתנת לרוב בתחילת המחלה כשהתסמינים קלים, או בשלבים מתקדמים – כשנמצא שהיא מועילה לטיפול בתופעה מאוחרת של פרקינסון של 'קיפאון בהליכה'. תופעות הלוואי של התרופה כוללות שינויים בצבע העור, נפיחות בעקב והזיות.
- אנטגוניסטים לקולטני אדנוזין
התרופות מקבוצת האנטגוניסטים לקולטני אדנוזין, המכונות גם 'אנטגוניסטים לקולטני A2A', מכוונות לפעילות על אזורים במוח שמווסתיים את התגובה של המוליך העצבי דופמין, באופן שמוביל להפרשה מוגברת של החומר ועלייה בריכוזו במוח. בקבוצה זו התרופה עם החומר הפעיל איסטרדפילין, שאיננה משווקת בישראל.
תופעות הלוואי השכיחות כוללות הזיות ותנועות חוזרות ובלתי רצוניות של השפתיים, הלשון, הזרועות והרגליים.
בקהילה הרפואית והמדעית תולים בשנים האחרונות תקוות בטיפולים שנמצאים עדיין בשלבי מחקר שמבקשים לטפל בעתיד בפרקינסון בהתאם לנשאות של מוטציות גנטיות, תוך שינוי של השפעות המוטציות או החדרה של גנים תקינים, באופן שיוביל לשיקום תאי עצבים במוח, הצטברות גורמי גדילה שיגנו על תאי העצב מנזקים ושליטה בתסמיני המחלה.
טיפולים נוספים לפרקינסון
לצד התרופות, במצבים מתקדמים שבהם לא ניתן עוד לשלוט בתסמיני פרקינסון באמצעים תרופתיים – נדרש לעתים לעבור טיפולים פולשניים.
- השתלת קוצב וגירוי מוחי עמוק
הניתוח הנפוץ ביותר לפרקינסון קרוי 'גירוי מוחי עמוק' (DBS, קיצור של Deep Brain Stimulation), ובמהלכו משתילים נוירוכירורגים (מנתחי מוח) אלקטרודות באזורים ספציפיים במוח ששולטים על התנועה, ואלה מקושרים לקוצב שמוצמד מתחת לעור לעצם בית החזה. הקוצב משגר אותות חשמליים דרך האלקטרודות באופן שמסייע להתמתנות התסמינים של פרקינסון. ההליך מתאים למטופלים עם פרקינסון בשלבים מתקדמים בהם התועלת של הטיפול בלבודופה דועכת ואינה יציבה, והוא מועיל הן להפחתת תנועות לא רצוניות (דיסקינזיה) ונוקשות שרירים ולשיפור התנועתיות ובייחוד להפחתת רעידות.
הטיפול כלול בישראל בסל הבריאות הממלכתי לפרקינסון ורעד קשה העמידים לטיפול תרופתי בהמלצת נוירולוג. יש לציין כי הטיפול אינו מסייע לעכב תהליכי דמנציה ואף עלול להחמירם. מעבר לכך, חשוב להדגיש כי גם גירוי מוחי עמוק אינו מאפשר לבלום לחלוטין את התקדמות מחלת הפרקינסון. לדברי ד"ר יהלום, "הטיפול אינו מתאים לכלל החולים, אך בהחלט עשוי להיות מועיל בחלק מהמקרים".
- אולטרה סאונד ממוקד להפחתת רעד
אחד הטיפולים ברעידות אצל המאובחנים עם פרקינסון ניתן באמצעות גלי על-קול – אולטרה-סאונד לאזורים ספציפיים במוח שמהווים מקור לרעד, והוא מבוצע תחת הדמיה מסוג MRI (הטיפול קרוי MRgFUS). גלי האולטרה סאונד למעשה שורפים את האזורים שתורמים להתפתחות הרעד, וכך ממתנים את עוצמתו.
הטיפול כלול בישראל בסל הבריאות הממלכתי בהמלצת נוירולוג לסובלים מאבחנה של 'רעד ראשוני', אולם ההנחה כי בהמשך יוצע גם לפרקינסון.
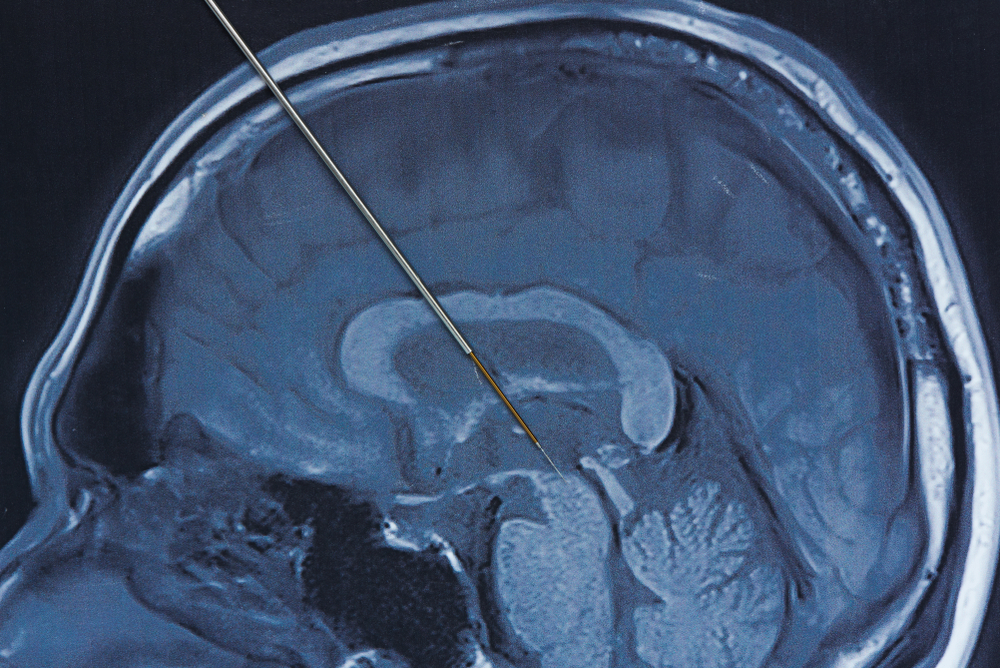
הדמיית ניתוח נוירוכירורגי להשתלת קוצב מוח למוקד הרעד (צילום: Shutterstock)
החיים עם פרקינסון
לצד הטיפולים התרופתיים והנוספים בפרקינסון, חשוב לשים לב להיבטים של שמירה על איכות חיים טובה תחת עקרונות של אורח חיים בריא.
- פעילות גופנית: למאובחנים עם פרקינסון מומלץ להקפיד על פעילות גופנית סדירה אירובית קבועה שהוכחה כמועילה בעיכוב התקדמות המחלה.
- תזונה בריאה: אמנם אין כיום דיאטה ספציפית שהוכחה כמועילה לאנשים עם פרקינסון, אולם ככלל מומלץ על תזונה בריאה, ובמחקרים זוהו מספר פרטי מזון שעשויים להקל בתסמינים, ובהם: אכילת פירות וירקות העשירים בסיבים תזונתיים ושתייה מרובה של נוזלים למניעת עצירות; הקפדה על צריכת חומצות שומן מסוג אומגה 3 המצויות בעיקר בדגים מהים הצפוני, אגוזים ושקדים; וצריכת קפאין שהוא כאמור בעל השפעה מגנה אפשרית מפני פרקינסון.
- גמילה מעישון: הפסקת עישון סיגריות היא המלצה כללית למאובחנים עם מחלות כרוניות, אם כי יש לציין כי בפרקינסון נצפה במחקרים 'פרדוקס עישון' שהו מעשני סיגריות דווקא מוגנים יותר מפני המחלה ומהחמרתה, וזאת אולי כתוצאה מהשפעה כלשהי של כימיקלים בסיגריות על עיכוב התקדמות המחלה. יחד עם זאת, למרות שמחקרים מצאו כי מאובחנים עם פרקינסון שמעשנים סיגריות פחות נוטים לתמותה על רקע תחלואה נוירולוגית – מתברר כי לחולים אלה יש נטייה לתמותה ממחלות שקשורות לעישון, כמו סרטן הריאות.
- טיפולים במקצועות הבריאות: ניתן להיעזר בטיפולי פיזיותרפיה ששמים דגש על מתיחות ואיזון שווי המשקל בגוף ובטיפולי קלינאות תקשורת שמסייעם לשפר בעיות בדיבור ובשלבים מאוחרים של המחלה גם בעיות בבליעה.
- תמיכה נפשית: הקשר ההדוק בין פרקינסון לפגיעה במצב הנפשי ובעיקר לדיכאון מחייב לעתים פנייה לעזרה נפשית מקצועית שביכולתה לתמוך בחולים ולספק להם כלים להתמודדות עצמית.
- רפואה משלימה: מחקרים רומזים כי מספר שיטות של רפואה משלימה מסייעות להקל בתסמינים של פרקינסון, ובכללם עיסוי שמסייע להפחית מתח ומעודד הרגעות; טאי צ'י שמסייע לשיפור הגמישות והיציבה ועשוי למנוע נפילות; יוגה שמשפרת את היציבה; שיטת/ טכניקת אלכסנדר שמסייעת ליציבות השרירים ומפחיתה מתח וכאבים; מדיטציה שמסייעת להפגת מתחים וכאבים ולשיפור איכות החיים הכוללת; ואפילו טיפול בבעלי חיים שתורם לגמישות ולתנועתיות ולשיפור בהיבטים רגשיים.
ד"ר גלעד יהלום הוא מנהל היחידה להפרעות תנועה במרכז הרפואי שערי צדק ויו"ר החברה הישראלית להפרעות תנועה
עדכון אחרון: מארס 2024

