צנתור לב – כל הפרטים
מהו צנתור לב? מתי הוא נדרש? איך הוא מבוצע? מה הסיכונים בצנתורים? ומה צפוי לאחר צנתור? מדריך
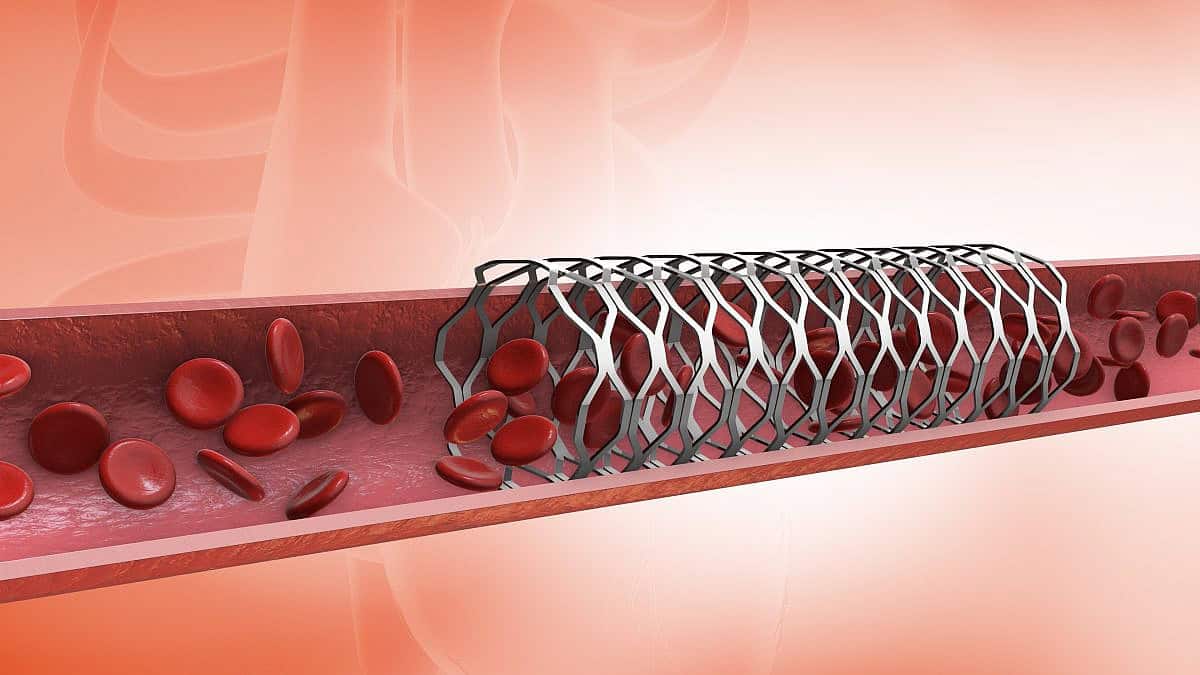
צנתור לב (Heart/ Cardiac Catheterization) מהווה פעולה רפואית שבמסגרתה מוחדרת צינורית קטנה (בקוטר 2 מ"מ) דרך עורק ביד או ברגל ללב. דרך הצינורית מוזרק חומר ניגוד אשר מאפשר לרופא להדגים בעיות בכלי הדם. לדברי פרופ' ירון ארבל, רופא בכיר ביחידת צינתורים ומנהל המרכז למחקר קרדיווסקולרי במרכז הרפואי תל אביב ע"ש סוראסקי (איכילוב), "צנתור מוגדר כפעולה פולשנית שאינה ניתוחית, כלומר שהיא אינה מערבת חתכים והרס רקמות ואינה דורשת תהליך שיקומי כמו ניתוח".
צנתור לב עשוי להיות אבחנתי – כדי להעריך את הנזק לכלי הדם ו/או טיפולי – כשהוא מלווה בטיפול בנזק שזוהה. בשנים האחרונות מבוצעים גם צנתורים לטיפול במחלות קרדיו וסקולאריות גם מעבר לפתיחת עורקים חסומים, בין השאר לטיפול במחלות במסתמי הלב ותיקון מומי לב.
צנתורי לב מבוצעים על ידי רופאים קרדיולוגים, בהבדל מניתוחי לב שמבוצעים על ידי רופאים מומחים בכירורגית לב-חזה. במקרים מורכבים נהוג בשנים האחרונות בחלק מבתי החולים בארץ לקיים היוועצות מולטי דיסציפלינארית משותפת לקרדיולוגים ולמנתחי לב כדי לקבוע את התוכנית הטיפולית המומלצת בצנתור או בניתוח לב.
צנתורי לב לרוב מבוצעים בהרדמה מקומית בלבד, ואינם מערבים כאבים עזים, אם כי הפעולה עשויה לגרום לנפיחות וכאב קל בכלי הדם אליו הוחדר הצנתר, ובמקרים נדירים עלולה להוביל לסיבוכים קשים.
הכתבה הבאה מפרטת על היבטים הקשורים בצנתורי לב:
סוגים של צנתורי לב
קיימים סוגים שונים של צנתורי לב הנחלקים לשתי קטגוריות מרכזיות:
- צנתורים אבחנתיים שמטרתם לאבחן בעיות/פתולוגיות בכלי דם.
- צנתורים טיפוליים שמטרתם לטפל באותן בעיות/ פתולוגיות.
בצנתור אבחנתי, הצנתר משמש לאבחון החסימה בעורק, למשל באמצעות החדרת חומר ניגוד שמבוסס על יוד שמאפשר סימון של אזורים מוצרים/חסומים בצילום רנטגן או על ידי מצלמות מיוחדות שמבוססות על אולטרה סאונד או סיב אופטי שמאפשר צפייה בכלי הדם מבפנים; ובצנתור טיפולי משמש הצנתר לטיפול בפתיחת היצרות/חסימה בכלי הדם. הצנתר מוחדר לגוף לרוב דרך היד, ולעתים דרך המפשעה – כפי שהיה נהוג בעבר.
לרוב, תחילה מבוצע צנתור אבחנתי, ולאחר שמזוהה חסימה מסוכנת בעורק – מתבצע בהמשך צנתור טיפולי לפתיחת החסימה באותה הפעולה.

צנתור לב אבחנתי
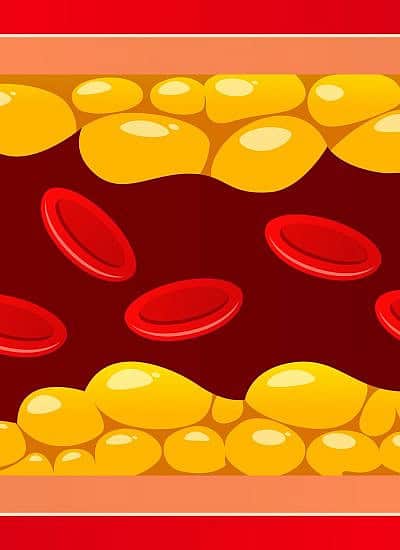
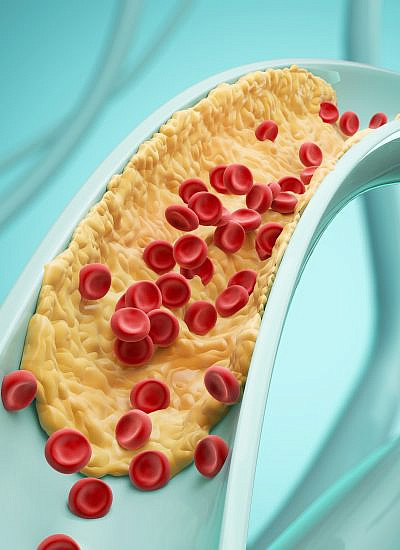
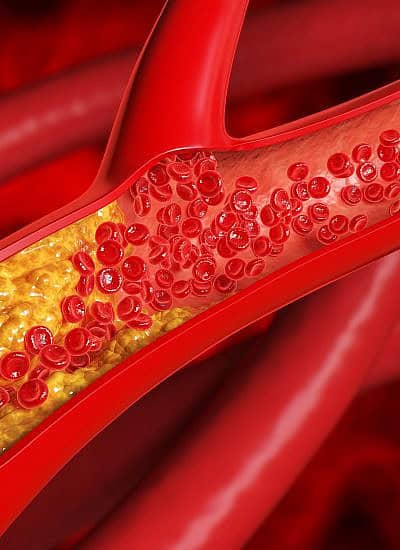
צנתור אבחנתי נדרש כדי להעריך את מצב כלי הדם במקרים של הופעת תסמינים המעלים חשד לחסימה בכלי דם/ אירוע לב, בעיקר כאבים בחזה. צנתור במקרה זה מאפשר לבחון האם עורק המוליך כלי דם ללב נחסם באופן חלקי או מלא על ידי הצטברות רובד טרשתי – מצב המוגדר כטרשת עורקים.
לאחר צנתור אבחנתי – יש 3 אפשרויות, הראשונה, שלא נמצאות היצרויות משמעותיות ולכן מומלץ טיפול שמרני שכולל אורח חיים בריא בשילוב של תרופות. האפשרות השניה, היא שנמצאות היצרויות אשר בהמשך ייתפתחו על ידי תומכנים (סטנטים). במקרים מורכבים עם ריבוי היצרויות, המטופלים מופנים לניתוח מעקפים.
צנתור לב מבוצע לעתים גם לצורך בירור פעילות הלב ולאבחון ליקויים שונים במסתמי הלב האחראים להכוונה נכונה של זרם הדם לתוך הלב ובהמשך לגוף. וכן לאבחון לקויים בשריר הלב, קרומי הלב ומומים מולדים בלב. צנתור לב עשוי לשמש גם למדידת קצב זרימת הדם ורמות החמצן בדם באזורים שונים בלב או ריאות , כדי להעריך נכונה כיצד מתפקד הלב כמשאבת הדם של הגוף. צינתורים אלו נקראים צינתורים ימניים או צינתורי ריאות.
קבוצה נוספת של מטופלים בהם מומלץ לשקול לבצע בירור מעמיק היא של בריאים שמוערכים בסיכון גבוה למחלות לב/התקפי לב על רקע תסמינים שונים וגורמי סיכון, לרבות היסטוריה משפחתית של מחלות לב וכלי דם בגיל צעיר, עישון, ערכים גבוהים של שומנים בדם, סוכרת, יתר לחץ דם, השמנת יתר ואי הקפדה על פעילות גופנית סדירה. במקרים כאלו, החולים מופנים לצנתור וירטואלי, שהוא למעשה הדמיית סי.טי של הלב וכלי הדם,
צנתור לב ככלי אבחנתי מהווה רק בדיקה אחת מתוך מגוון בדיקות אבחנתיות לליקויים בפעילות הלב וכלי הדם, הכוללות גם מבחן מאמץ, מיפוי לב במאמץ ואקו לב במאמץ וכן בדיקות אבחנתיות נוספות שהצורך בביצוען נקבע בהתייעצות עם הקרדיולוגים.
איך מבוצע צנתור אבחנתי?
בצנתור אבחנתי, מוחדר הצנתר לכלי הדם, כיום לרוב דרך שורש כף היד ולעיתים דרך המפשעה, לרוב בהרדמה מקומית. הצנתר הוא למעשה צינור פלסטיק דקיק בקוטר של כ-2 מ"מ המכיל בתוכו תיל קפיצי המאפשר לו גמישות, שמוחדר בעדינות עד לעורקי הלב.
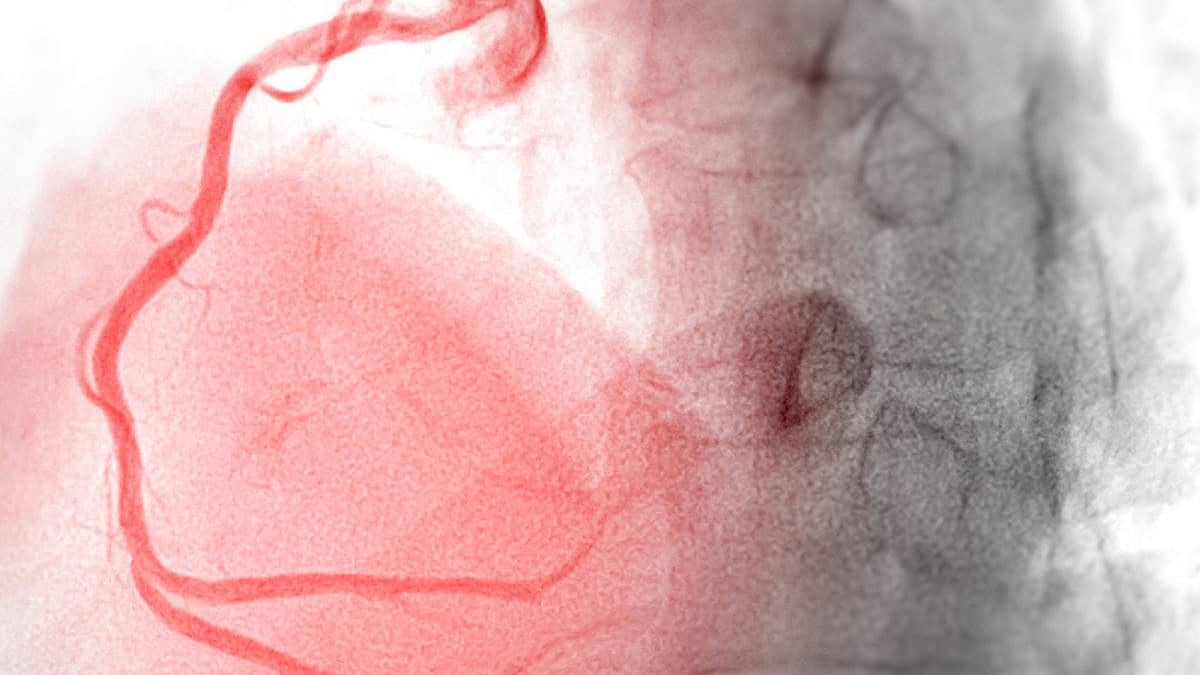
בהליך האבחנתי מוחדר דרך הצנתר חומר ניגוד לשלושה מעורקי הלב של המטופל, המאפשר לצבוע אזורים בהם מתפתחת חסימה של כלי הדם על ידי רובד טרשתי. בהמשך מתבצע צילום רנטגן הקרוי 'אנגיוגרפיה', במהלכו ניתן לזהות את אזורי ההיצרויות והחסימות בעורקים המוליכים דם ללב ולאפיין את דרגת חומרתן.
כיום יש עדיפות לצנתור דרך העורק הרדיאלי ביד שכרוך בפחות סיבוכים של דימום מאשר צנתור במפשעה ובנוחות גבוהה יותר למטופלים.
צנתור וירטואלי
צנתור וירטואלי אינו מהווה צנתור. המדובר בכינוי העממי של בדיקת הדמיה אבחנתית של כלי הדם מסוג סי.טי לב שאינה פולשנית, וזאת בהבדל מצנתור, תוך הזרקת חומר ניגוד לגוף ללא צורך בהחדרת צנתר.
צנתור לב טיפולי
במקרים בהם מאובחן רובד טרשתי בעורקים עשויים הקרדיולוגים לעבור מיד לצנתור טיפולי לצורך פתיחת העורק – פעולה המכונה בעגה הרפואית 'התערבות כלילית מלעורית (PCI, קיצור של Percutaneous Coronary Interbention) ומכונה לעתים גם 'אנגיופלסטיה'.
בעשורים האחרונים, צנתור ראשוני של חולים עם אוטם שריר הלב חריף הפך לפעולה רפואית מועדפת עם שיעורי הצלחה גבוהים בפתיחת העורק הסתום בהשוואה לטיפולים מסורתיים במדללי דם ותרופות נוגדות קרישה.
איך מבוצע צנתור טיפולי?
צנתור מבוצע לרוב בהרדמה מקומית, ובחלק מהמרכזים הרפואיים מטופלים אף יכולים לבחור את המוסיקה שתושמע בחדר בעת ביצוע הפעולה.
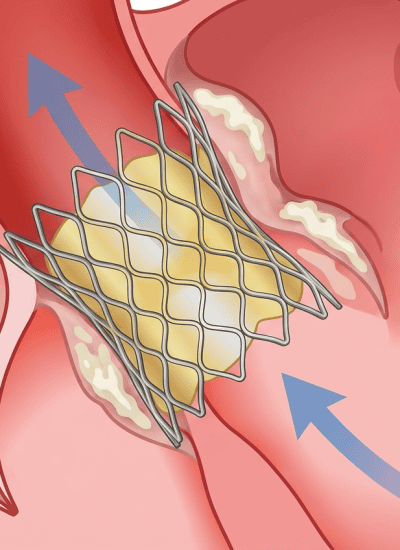
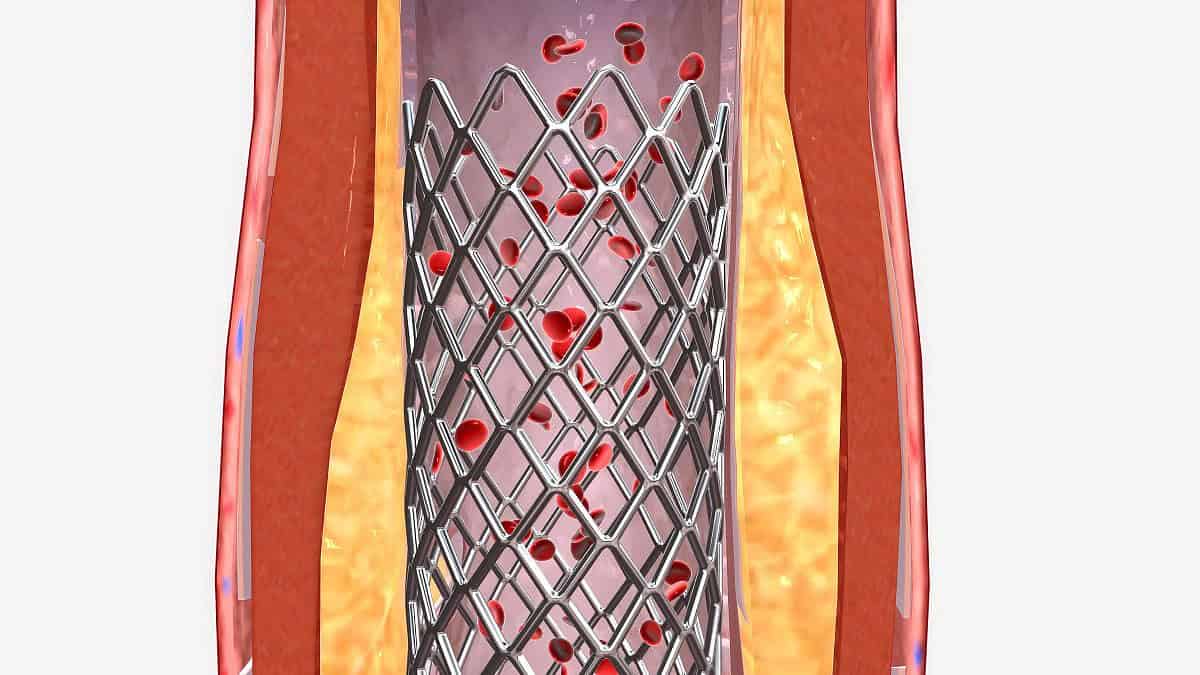
גם בצנתור טיפולי מוחדר הצנתר לגוף דרך שורש כף היד ולעתים חריגות דרך המפשעה. הצנתר מכיל תיל קפיצי המקנה לו גמישות וכן בלון שמועבר בעדינות אל העורק החסום. כשהצנתר מיוצב באזור החסימה, הבלון מנופח – לקוטר של 3 מ"מ בממוצע – כך שהוא הודף את הרובד הטרשתי החוסם כנגד קירות כלי הדם ומייצר מעבר רחב יותר לזרימת הדם.
בשיעור בודד מהמקרים ניתן להסתפק בפעולה זו (פחות מ-5%), אולם ברוב המכריע של הצנתורים הטיפוליים מוחדר בהמשך דרך הצנתר סליל (סטנט/ תומכן) שתומך את פנים כלי הדם לאחר שחרור הזרימה שבוצע באמצעות הבלון.
בעבר שווקו מספר סוגים של סטנטים ששימשו לצנתורי לב. כיום נעשה שימוש בעיקר בסטנטים מצופי תרופות (DES, קיצור של Drug-Eluting Stents), שמטרתן להפחית את הסיכון לסתימה חוזרת של העורק ולצורך בצנתור נוסף. השיקולים בבחירת הסטנט נעשים בהתייעצות עם הקרדיולוגים, ומבוססים על נתוני החולים, מצבם הנוכחי ומאפיינים של העורק המטופל (לרבות קוטרו של העורק ואופי ההיצרות).
רוב הסטנטים בשימוש כיום עשויים מתכת קובלט-כרום או פלטינה-כרום, ורובם מצופים בפולימר – כלומר שכבה מיקרוסקופית בתוכה מצויה תרופה המופרשת בשחרור איטי אשר מונעת היצרות חוזרת. ברוב הסטנטים נעשה שימוש בתרופות מקבוצת מעכבי mTOR המעכבות את ההתרבות (פרופילרציה) של תאי שריר חלק בדופן כלי הדם, כגון אברולימוס, זוטרולימוס, ביולימוס וסירולימוס. בחלק מהסטנטים הפולימר נותר על הסטנט גם לאחר הפרשת התרופה, ובסטנטים מהדור החדש הפולימר מתכלה ונעלם כעבור מספר חודשים, או שנעשה שימוש בפולימר ביולוגי. לעתים נעשה שימוש בסטנטים המצופים תרופות באופן ישיר וללא שימוש בפולימר.
במקרים מורכבים עם היצרויות חוזרות בתוך תומכנים ישנים, ניתן לעשות שימוש בבלון מפריש תרופה למניעת היצרות חוזרת של העורק, אשר אינו מצריך בהמשך הכנסת סטנט/תומכן.
שכיחות של צנתורים
לפי נתונים שנאספים ברשם הצנתורים במרכז הלאומי לבקרת מחלות שבמשרד הבריאות, בשנים האחרונות מבוצעים מדי שנה מעל ל-50 אלף צנתורי לב בישראל.
במהלך שנת 2023 בוצעו בארץ 54,973 צנתורי לב, מתוכם 53,004 צנתורים בעורקים הכליליים שמוליכים דם ללב – כמחציתם (48.5%) הוגדרו כצנתורים אבחנתיים (25,727 צנתורים), וכמחציתם (51.5%) צנתורים טיפוליים (27,277 צנתורים).
בהשוואה על ציר הזמן, תוך 15 שנה מתועדת עלייה של 25.9% במספר צנתורי הלב, בהשוואה ל-43,674 צנתורי לב בשנת 2008. בבחינת שיעור הצנתורים ביחס לגודל האוכלוסייה – משנת 2008 עד 2018 תועדה ירידה בשיעור הצנתורים, ומאותה השנה נרשמת מגמת עלייה, ונכון לשנת 2023 עמד השיעור על 570.7 צנתורי לב לכל מאה אלף ישראלים.
נכון לשנת 2023, מבין הצנתורים האבחנתיים – רק במיעוט מהמקרים (1.2%) נדרשה הוצאת דגימת ביופסיה מכלי הדם או הלב (335 ביופסיות). כמו כן, בהיקף נמוך של צנתורים אבחנתיים (5.9%) בוצע צנתור אבחנתי המודינמי, צינתור ימני או צינתור ריאות , שמטרתו להעריך לחצים והפרשי לחץ בעליות וחדרי הלב ובעורקים, בין השאר להערכת לקויות ומחלות במסתמי הלב, אבחון אי ספיקת לב, אבחון יתר לחץ דם ריאתי, אבחון מומי לב מולדים והערכה לפני ניתוח לב או השתלת איברים (1,634 צנתורים).
מבין הצנתורים הטיפוליים – קרוב למחצית (45%) בוצעו לחולים עם תחלואת לב יציבה (12,274 צנתורים), ומעל למחצית (55%) לחולים עם תחלואת לב לא יציבה, כלומר לאחר אירוע לבבי על רקע חסימה של זרימת הדם ללב בעורק/ים כלילי/יים (15,003 צנתורים). ברוב המכריע של הצנתורים הטיפוליים (89.3%) הושתל תומכן (סטנט) מצופה תרופה מסוג DES אחד לפחות לפתיחת העורק החסום (24,368 צנתורים). כעשירית מהצנתורים הטיפוליים (10.2%) בוצעו באמצעות החדרת בלון לפתיחת העורק החסום – בלון רגיל או מצופה תרופה (2,772 צנתורים). במיעוט מזערי מהצנתורים הטיפוליים (0.5%) הוחדר תומכן מתכתי רגיל לפתיחת העורק החסום ללא ציפוי בתרופה – הליך שמבוצע במקרים בהם קיימת רגישות לתרופות (1378 צנתורים). מבין הצנתורים הטיפוליים בשנת 2023 – בוצעו 3,388 צנתורים טיפוליים מבניים – שמטרתם לטפל במחלות מסתמים ומומי לב.
בבחינת שיעור צנתורי הלב הטיפוליים באוכלוסייה למיליון תושבים, כפי שנאסף על ידי החברה האירופית לקרדיולוגיה (ESC), ובהתבסס על נתוני השנים 2023-2020, השיעורים הגבוהים ביותר מתועדים בבולגריה (5,050 למיליון), גרמניה (4,008.8 למיליון), תורכיה (3,822.2 למיליון), וכן בלטביה, ליטא וארמניה, ישראל ממוקמת במרכז הדירוג (2,800.9 למיליון), מתחת לצרפת (3,164.8 למיליון) ומעל לבריטניה (1,459.8 למיליון), ובתחתית אלג'יריה (512.2 למיליון), תוניס (342 למיליון) ואוזבקיסטן (336.6 למיליון), כאשר ארה"ב אינה מיוצגת בדירוג.
צנתור או ניתוח מעקפים
אחד הדיונים הפוריים בקהילה הרפואית בשנים האחרונות נוגע לעלייה בשימוש בצנתורים ככלי לטיפול בהיצרויות בלב, תוך החלפת ניתוחי מעקפים – ניתוחי לב הרואיים שבוצעו בעבר. לפי מחקר השוואתי שנערך ב-16 מדינות עם רמה סוציואקונומית גבוהה, שלא כלל את ישראל, אשר ממצאיו פורסמו בדצמבר 2025 בכתב העת BMJ Open, נמצא כי בין השנים 2006 ל-2020 תועדה עלייה בשיעור הצנתורים ברוב המדינות (11), ובעיקר עלייה של 36% בפינלנד, עלייה של 34.5% באירלנד ועלייה של 31.5% בצרפת, לצד ירידה בשיעור ניתוחי הלב ברוב גדול יותר של מדינות (14), ובעיקר בלוקסמבורג (ירידה של 71.3%), בריטניה (ירידה של 62.6%) ופינלנד (ירידה של 60.6%). לפי מחקר ישראלי שפורסם בפברואר 2017 בכתב העת JAHA היוצא לאור מטעם איגוד הלב האמריקאי, נמצא כי שיעור צנתורי הלב עמד בשנת 2014 על 378.5 הליכים לכל מאה אלף איש, שיעור דומה לזה שתועד בשנת 2002, ואילו באותם השנים ירד ב-59% שיעור ניתוחי המעקפים (מ-109 ל-45.2 ניתוחים לכל מאה אלף איש).
כיום ברוב התקפי הלב מופנים הנפגעים לטיפול באמצעות צנתור, אולם במצבים מסוימים – כשהתועלת גוברת על הסיכון – מופנים הנפגעים לניתוח מעקפים, ובעיקר במצבים הבאים:
- חסימות רבות במספר עורקים
- חסימות מורכבות
- יש מעורבות בחסימת העורק השמאלי הראשי של הלב
- חולים עם סוכרת
במצבים אלו הסיכון הכרוך בצנתור מוערך לרוב כגבוה מזה של ניתוח מעקפים.
כאמור, כיום קיימים מרכזים רפואיים שבהם נוצרים צוותים רב מקצועיים בהם משתפים פעולה מנתחי לב וקרדיולוגים בהחלטה האם לבצע צנתור או ניתוח מעקפים בחולים שנפגעו מאירוע לבבי.
צנתור טיפולי דחוף לעומת מתוכנן
במקרים של חסימה חלקית בעורק המזוהה בבדיקה אבחנתית, למשל בעקבות אנגינה פקטוריס (תעוקת חזה), נהוג לבצע צנתור לב טיפולי מתוכנן, אם כי במצבים אלה קיימת מחלוקת בקהילה הרפואית באשר לצורך לבצע גם צנתורי לב טיפוליים מתוכננים, ויש רופאים שטוענים כי ניתן להסתפק בטיפול תרופתי שאינו פולשני באמצעות תרופות להמסת קרישי דם – באחוזי יעילות דומים.
"כדי לקבוע כיום צנתור לב טיפולי מתוכנן, לא מספיק להעריך שהסתימה שזוהתה בכלי הדם תיפתח, אלא יש לקבוע גם שאספקת הדם לשריר הלב תשתפר כתוצאה מכך", מדגיש פרופ' ארבל.
במצבים בהם צנתור מזהה חסימה בכלי דם במקרה של אירוע לב חריף או היווצרות קריש דם מעל החסימה, המהווה סיכון להתקף לב חריף – נדרש צנתור דחוף המהווה טיפול עזרה ראשונה מציל חיים, ששיעורי ההצלחה שלו בפתיחת כלי הדם עומדים כיום על כ-98% וגבוהים יותר בהשוואה לשיעורי ההצלחה של טיפול בתרופות (50% עד 70%) במצבים אלה. צנתור דחוף מוגדר ככזה המבוצע תוך 12 שעות מתחילת הופעת תסמיני התקף הלב.
כיום כ-80% מהחולים שעוברים התקפי לב מופנים לצנתור דחוף, ומוערך כי בקרב 60% מהחולים שעוברים צנתור לב אבחנתי – זה הופך בהמשך לצנתור טיפולי לתיקון הליקויים שאותרו בשלב האבחנתי. שיעורי ההצלחה הגבוהים בהפניית חולי לב לצנתורים דחופים הם לפי קהילת הקרדיולוגים המקור העיקרי לירידה בתמותה מהתקפי לב בישראל בשנים האחרונות – כשסרטן עקף את מחלות הלב והפך בשנים האחרונות לגורם התמותה המוביל במדינות המערב, לרבות ישראל.
צנתורים מיותרים
נתונים ממחקרים בשנים האחרונות מעלים כי ב-10% מהמקרים שמפונים לצנתור על רקע סימני התקף לב, מתברר בהמשך כי החולה לא פיתח התקף לב והצנתור היה למעשה מיותר. זאת מאחר וקיימים מצבים בבדיקת אק"ג שעשויים להטעות ולהציג תמונה של התקף לב, כמו למשל במקרים של דלקת שריר הלב.
התפיסה כי נעשים צנתורי לב מיותרים בחולים שאין צורך לבצע בהם טיפול פולשני, זכתה לגיבוי חלקי במספר מחקרים, בהם מחקר שפורסם במארס 2010 בכתב העת New England Journal of Medicine שזיהה ברשם הלאומי לצנתורים אלקטיביים בארה"ב, כי לפי נתונים שנאספו מהשנים 2008-2004, אצל מעל לשליש מהנבדקים שעברו צנתור (39.2%) לא נמצאו במסגרת ההלך סימנים לטרשת עורקים. במחקר מעורר הדים שפורסם עוד בשנת 2007 באותו כתב העת, שכונה מחקר COURAGE, נבדקו 2,287 חולי לב יציבים מארה"ב וקנדה, שחלקם טופלו במשולב בצנתור ותרופות לפתיחת עורקים סתומים וחלקם טופלו בתרופות בלבד. בעוד שהנחת החוקרים הייתה כי הרחבת העורקים בצנתור היא הטיפול המיטבי בחולים, לאורך מעקב שנמשך עד שבע שנים היו שיעורי הצלחה זהים בשתי הקבוצות להפחתת הסתימות בעורקים, ולא נמצא הבדל בין הקבוצות בשיעורי התמותה והיארעות התקפי לב. מאידך, המטופלים ציינו כי הרגישו טוב יותר.
הממצאים הובילו בשנים האחרונות להרחבת השימוש בבדיקה מסוג FFR (קיצור של Fractional Flow Reserve), המודדת את זרימת הדם בכלי הדם החסום ומאפשרת לקבוע רפואית האם יש צורך בצנתור טיפולי, או שניתן להסתפק בטיפול תרופתי כנגד החסימה וכך להימנע מטיפול פולשני כמו גם לחסוך כסף למערכת הבריאות. בדיקת FFR מחשבת למעשה במהלך הצנתור האבחנתי את הלחץ בעורק לפני ואחרי הצנתור בזמן שהלב במצב של עומס מירבי, וזאת באמצעות הזרמת תרופה להרחבת כלי הדם. הבדיקה מאפשרת לבחון אם ההיצרות פוגעת בזרימת הדם בצורה משמעותית, וכאשר היחס בין הלחץ הדיסטלי (אחרי ההיצרות) לבין הלחץ הפרוקסימלי (לפני ההיצרות) נמוך מ-0.80 – יש סבירות גבוהה שההיצרות משמעותית, ולרוב המטופלים יופנו לצנתור לב טיפולי.
ההכנות לפעולה
לפני ביצוע צנתור, על המטופל/ת לדווח על רגישות לתרופות ובמיוחד רגישות ליוד המוזרק דרך הקטטר בצנתור האבחנתי, כדי למנוע תגובה אלרגית.
כמו כן, בחלק מהמקרים יש צורך בהפסקה זמנית של תרופות לפני ביצוע צנתור, לרבות מדללי דם ותרופות לסוכרת. כהכנה לצנתור נדרשות גם בדיקות מעבדה עדכניות, לרבות ספירת דם ותפקודי כבד וכליות.
מטופלים עם אי ספיקת כליות זקוקים להכנה מיוחדת לקראת צנתור המבוצעת בהזלפת נוזלים לווריד, כדי לצמצם את הסיכון להחמרה במצב הכליות עקב השימוש בחומר ניגוד במהלך הפעולה.
לפני צנתור טיפולי יש הכרח לתת למטופלים מדללי דם, כדי למנוע התפתחות קריש דם בתומכן שמוחדר לעורק לאחר פתיחתו. כיום נהוג לתת מדללי דם גם לפני צנתור אבחנתי, מתוך הנחה כי הוא עשוי להפוך בהמשך לטיפולי. כשש שעות לפני צנתור מתוכנן נהוג לתת תרופות לדילול דם מסוג אספירין ופלביקס, ולפני צנתור דחוף על רקע אירוע לב חריף ניתנים אספירין וכן ברלינטה/ אפיאנט.
סיבוכים של צנתורים
צנתור לב עלול להיות כרוך בסיבוכים, כמו כל פעולה רפואית פולשנית אחרת, אך נחשב ככלל לפעולה בטוחה יחסית.
בצנתור אבחנתי הסיכון לסיבוך נאמד בהרבה פחות מ-1%, ואילו בצנתור טיפולי, במהלכו מועברים בלון וסליל דרך הקטטר – הסיכון לסיבוכים נאמד בפחות מ-3%.
סיבוכים שכיחים בצנתורי לב כוללים:
- דימום תת עורי, זיהום או כאב במקום החדרת הצנתר. יש לציין כי בשנים האחרונות, כשצנתורי לב מבוצעים לרוב דרך שורש כף היד, חלה ירידה משמעותית בסיכון לדימומים בהשוואה לצנתורים בעבר שבוצעו דרך המפשעה.
- פגיעה בכלי הדם בעת החדרת הקטטר שעלולה לגרום לדימום, קרע או חור בעורק המטופל ולעתים אוטם שריר הלב – סיבוך שנחשב חריג ביותר.
- במהלך צנתור עלולה להתפתח תגובה אלרגית לחומר היוד שמוחדר לבדיקת מצב כלי הדם וטרשת העורקים.
סיבוכים שאינם שכיחים של צנתורי לב כוללים:
- במהלך צנתור לב עלול התומכן (סטנט) המוחדר לאחר פתיחת העורק לגרום להיווצרות קריש דם שעלול להיות קטלני ולגרום בהמשך להתקף לב או שבץ מוחי. למניעת סיכון זה נהוג לטפל בתרופות לדילול הדם לפני הצנתור.
- הפרעה בקצב הלב מסוג אריתמיה שלרוב חולפת מעצמה ולעתים דורשת טיפול לאחר הצנתור.
- פגיעה בכליות על ידי היוד המוזרק במהלך הצנתור האבחנתי.
- לחץ דם נמוך.
- הצטברות דם או נוזל בשק המקיף את הלב, באופן העלול לפגוע בקצב הלב ולמנוע דופק תקין.
הסיכון להתפתחות סיבוכים במהלך צנתורים גבוה יותר בקרב מטופלים מבוגרים וחולים כרוניים, לרבות חולי אי ספיקת כליות וסוכרת. למיומנות הקרדיולוגים במקרים אלה חשיבות רבה להצלחת הצנתור.
צנתור וקרינה
צנתור הוא פעולה רפואית המערבת חשיפה לקרינה מייננת, אולם רשויות בריאות רבות בעולם, ובהן המובילות בארה"ב ובאירופה, קבעו כי הסיכון בחשיפה לקרינה נמוך לאין ערוך מהיתרונות של הצנתור בפתיחת כלי הדם ובהצלת חיים ומניעת תמותה מאירוע לב. כיום ההנחה כי לקרינה בצנתור משמעות אפסית במקרה של צנתור אחד או שניים.
לפי חוזר משרד הבריאות על קרינה מייננת בבדיקות דימות, צנתור לב וכלי דם שמבוצע למטרות אבחון וטיפול שווה ערך לחשיפה לקרינה בכ-1,000 עד 1,500 צילומי חזה. לעומתו, צנתור לב וכלי דם שהוא רק אבחנתי שווה ערך לחשיפה לקרינה בכ-500 עד 1,000 צילומי חזה.
מה צפוי לאחר צנתור?
צנתור אבחנתי וכן צנתור טיפולי מצריכים בתום הפעולה השגחה למספר שעות בלבד, ובחלק מהמרכזים הרפואיים משוחררים המטופלים לביתם תוך שלוש שעות בלבד. יש מרכזים רפואיים שנוהגים עדיין להשאיר את המטופלים לאשפוז של לילה לצורך השגחה לאחר צנתור.
במהלך ההשגחה לאחר הצנתור עוברים המטופלים בדיקות לדופק הלב ולחץ הדם – במטרה לאתר דימומים פנימיים שעלולים להיווצר כסיבוך של הפעולה.
בימים הראשונים לאחר הצנתור מומלץ שלא לבצע פעולות שמסכנות את אזור החדרת הצנתר בדימום, אם מדובר ביד או במפשעה, למשל הרמת משאות כבדים או פעילות ספורטיבית אינטנסיבית.
לאחר הצנתור מומלץ למטופל אימוץ אורח חיים בריא – כולל הפסקת עישון, תזונה בריאה ופעילות גופנית סדירה.
לאור הסיכון להתפתחות קרישי דם בקרב מטופלים שעברו צנתור טיפולי הכולל החדרת סטנט/תומכן גם שנים לאחר החדרתו, לפי ההנחיות הקליניות המקובלות בישראל, שפורסמו לאחרונה בשנת 2018 מטעם המכון לאיכות ברפואה של ההסתדרות הרפואית, נדרש המשך טיפול במדלל דם מסוג אספירין לכל החיים, וכן טיפול בתרופה פלביקס (לעוברים צנתור מתוכנן) וברלינטה/ אפיאנט (לעוברים צנתור דחוף) למשך חצי שנה עד שנה לאחר הצנתור. עם זאת, בקהילה הרפואית קיים ויכוח בנושא, ויש שטוענים כי ניתן לקצר את הטיפול למספר חודשים בלבד. במקרים בהם המטופלים נזקקים לעבור לניתוח גדול – עליהם להפסיק את הטיפול בתרופות אלה המעלות את הסיכון לדימומים בניתוחים. עם זאת, לפני ניתוחים קטנים וטיפולי שיניים אין מגבלה להמשיך לקבל טיפול במדללי הדם.
- פרופ' ירון ארבל הוא רופא בכיר ביחידת צינתורים ומנהל המרכז למחקר קרדיווסקולרי (CVRC) במרכז הרפואי תל אביב ע"ש סוראסקי (איכילוב) ומנהל קהילת מחלות לב באתר כמוני
עדכון אחרון: פברואר 2026